Un hématome compliqué…

Il s’agit d’un patient de 29 ans, footballeur amateur, se présentant avec un hématome de la face antérolatérale de la jambe droite suite à un tacle “appuyé”. Le traumatisme date de 3 semaines, avec une évolution défavorable malgré le repos. Le patient ne rapporte aucun antécédent particulier ni aucune allergie. Il n’avait jamais décrit de symptomatologie au niveau de sa jambe auparavant. L’examen physique retrouve une tuméfaction de la face antérolatérale de la jambe en regard de la crête tibiale. Il n’existe pas de complications vasculo-nerveuses d’aval, la jambe est discrètement oedématiée. Le mollet est souple et indolore. La palpation de cette tuméfaction est peu douloureuse. La peau en regard est luisante, bombée, et une petite zone centimétrique violacée évoquant un début de nécrose cutanée à son sommet est apparue depuis quelques jours. Il n’existe pas d’adénopathies. Le patient est apyrétique.
Quiz 1 • D’après les données de l’examen clinique, quels examens complémentaires réalisez-vous ?
A. Aucun
B. Radiographie de la jambe droite face et profil
C. Échographie de la tuméfaction
D. Radiographie de la jambe droite face et profil et échographie de la tuméfaction
E. IRM de la jambe
Devant le caractère évolutif défavorable de cette lésion, une radiographie standard de première intention est indiquée pour éliminer une lésion osseuse sous-jacente. Celle-ci est strictement normale, ne retrouvant pas de lésion osseuse traumatique visible. Une échographie couplée au doppler a permis de mettre en évidence une collection probablement hématique, sans saignement actif au doppler. L’IRM est discutable dans ce contexte pour orienter le diagnostic et caractériser la tuméfaction au moindre doute sur une origine tumorale. Dans ce cas précis, l’aspect post-traumatique et l’apparition brutale sans autres antécédents orientent vers un hématome posttraumatique avec début de souffrance cutanée. Si la radiographie ou l’échographie dans des mains expertes avaient soulevé le moindre doute sur une origine non traumatique, une imagerie en coupe avec scanner et IRM aurait été indiquée. Le bilan a par ailleurs été complété par un bilan biologique avec NFS et CRP et ne retrouvait pas de syndrome inflammatoire biologique.
Réponse : D
Quiz 2 • Quelle stratégie thérapeutique proposez-vous ? (plusieurs réponses possibles)
A. Abstention thérapeutique et poursuite du repos sportif jusqu’à résorption de l’hématome
B. Traitement médical renforcé par glaçages pluriquotidiens, surélévation du membre inférieur, appui soulagé et bas de contention
C. Ponction de la collection
D. Drainage chirurgical
E. Anti-inflammatoires non stéroïdiens (AINS)
On propose dans un premier temps d’optimiser le traitement médical. Une ponction à 3 semaines d’un hématome organisé ne permettra pas de retirer un volume suffisant de liquide et présente peu d’intérêt. Les anti-inflammatoires ne sont pas indiqués, voire présentent un risque de surinfection secondaire de cet hématome. Le drainage chirurgical pourrait être proposé d’emblée.
Dans ce cas précis, le patient a été revu 1 semaine après l’optimisation du traitement médical, avec une majoration de la zone de “nécrose cutanée” de 2 cm de grand axe en regard de l’hématome. Nous avons donc posé l’indication d’un drainage chirurgical au bloc opératoire sous anesthésie locorégionale.
Après excision de la nécrose cutanée, nous avons drainé une collection d’aspect “gelée de groseille” d’un hématome vieilli. Devant la perte de substance cutanée liée à la nécrose, nous avons opté pour une cicatrisation dirigée de la plaie, compte tenu d’un sous-sol musculaire correct permettant de faire bourgeonner la plaie et d’envisager éventuellement dans un second temps une greffe de peau mince au besoin. De principe, le prélèvement a été adressé au laboratoire de bactériologie et d’anatomopathologie pour analyse. La culture prolongée est restée négative et le compte rendu anatomopathologique confirme l’hématome “banal”.
Malheureusement, après 1 mois et demi de soins locaux et de suivi hebdomadaire, l’évolution locale est restée défavorable, avec la persistance d’une perte de substance cutanée de près de 6 cm de grand axe (Fig. 1).
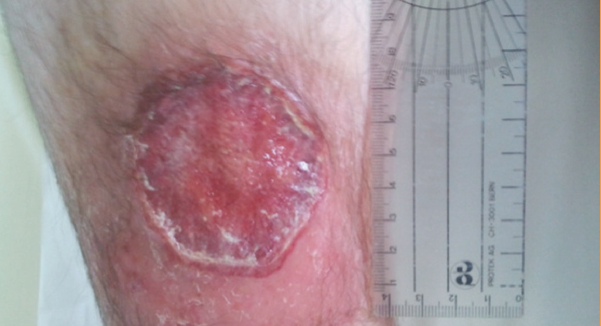
Figure 1 – Aspect de la lésion cutanée 1 mois et demi après la chirurgie.
Réponses : B et D
Quiz 3 • Quels diagnostics pouvez-vous évoquer devant ce retard de cicatrisation chez ce jeune patient, a priori sans antécédents ? (plusieurs réponses possibles)
A. Une primo-infection à VIH
B. Un diabète
C. Une insuffisance rénale chronique
D. Une insuffisance artérielle
E. Un tabagisme actif
F. Une hypoprotidémie
G. Une surinfection locale
Devant un retard de cicatrisation, il faudra rechercher une étiologie. L’ensemble de ces pathologies peut entraîner un retard de cicatrisation cutanée. Le bilan complet reste pourtant négatif chez notre patient et le recours à une prise en charge spécialisée en dermatologie a été nécessaire. En effet, cette lésion cutanée initiale violacée en regard de la collection n’était probablement pas une souffrance nécrotique liée à l’hématome, mais le point de départ d’une pathologie dermatologique plus générale.
Cette lésion arrondie, ulcérée à bordure et bourrelet inflammatoire, fibrineuse avec clapiers purulents périphériques, a nécessité une biopsie cutanée. Celle-ci a retrouvé un infiltrat neutrophilique dermique stérile. Ce faisceau d’arguments anatomocliniques a permis de conclure au diagnostic de pyoderma gangrenosum (PG) et a nécessité une prise en charge spécifique en dermatologie. Après traitement par corticothérapie orale et dermocorticoïde, la lésion a évolué lentement vers une cicatrisation, complète à 6 mois.
Réponses : A, B, C, D, E, F et G
Ce qu’il faut savoir sur le pyoderma gangrenosum
Le pyoderma gangrenosum est une dermatose neutrophilique inflammatoire stérile. C’est une pathologie rare, dont la prévalence exacte reste inconnue. On estime son incidence à 3 à 10 cas par million et par an. Il semble exister un pic entre 20 et 50 ans et une légère prédominance chez les femmes. L’étiologie est inconnue. Il existe 4 grands types anatomocliniques : ulcéreux (le cas de notre patient), bulleux, pustuleux et superficiel. Chaque type peut être associé. Le pyoderma grangrenosum ulcéreux est probablement le plus fréquent. Habituellement, il débute par des petites pustules ou un nodule sur peau saine, puis les lésions s’étendent et se creusent, évoluant vers une ulcération profonde, nécrotique et pseudo-purulente. L’urgence est alors d’éliminer une infection. Souvent, la lésion est douloureuse et ses bords sont violacés, irréguliers et oedémateux, avec des clapiers pustuleux à leur versant interne. Les lésions siègent aux membres inférieurs ou au tronc et leur évolution initiale est rapide et centrifuge. Le diagnostic est posé sur l’aspect clinique et évolutif de la lésion et sur la biopsie et étude en immunofluorescence directe. Il n’existe pas de critères diagnostiques formels et plusieurs auteurs ont proposé différents critères selon l’association de plusieurs arguments : aspect clinique de la lésion, exclusion des diagnostics différentiels (ulcérations vasculotrophiques, infectieuses, vascularites), histologie, maladies associées (maladies inflammatoires chroniques de l’intestin [MICI], polyarthrite rhumatoïde, hémopathie, gammapathie monoclonale), absence de diabète ou de maladie veineuse chronique, cultures bactériologiques négatives et réponse à un traitement systémique immunosuppresseur (von den Driesch 1997, Su et al. 2004, Marzano et al. 2011). Parfois, le bilan biologique retrouve une hyperleucocytose à polynucléaires neutrophiles. Dans 30 à 60 % des cas, il existe une association à une MICI, à une hémopathie maligne ou à une polyarthrite rhumatoïde, voire à certains cancers solides (côlon, prostate, poumon, sein). Le traitement repose actuellement sur la corticothérapie systémique ou locale dans les lésions très limitées. De nombreuses thérapeutiques sont en cours d’évaluation. La cicatrisation est obtenue en quelques semaines, laissant une cicatrice atrophique. Le traitement reste délicat, avec une évolution chronique actuellement difficilement prévisible en l’état des connaissances. Dans tous les cas, il faut considérer la prévention en raison du phénomène de pathergie de cette pathologie, en évitant les traumatismes locaux (perfusions, infiltrations, actes chirurgicaux…). Une prise en charge dans un centre spécialisé est toujours requise le plus tôt possible, dès l’étape diagnostique.
Conclusion
Cette expérience clinique permet de rappeler l’importance d’un diagnostic précis avant toute prise en charge thérapeutique. Une lésion “atypique” ou une évolution “inhabituelle” d’une présentation clinique paraissant “simple” doivent motiver le recours rapide à une prise en charge spécialisée dans le cadre d’un réseau coordonné de soins. Cet humble article n’a pas vocation à faire de chacun de nous des apprentis dermatologues, mais de mettre en lumière l’approche transdisciplinaire nécessaire à la pratique de la médecine du sport pour le bien du patient. Le pyoderma grangrenosum est une pathologie rare s’intégrant dans les dermatoses neutrophiliques nécessitant une prise en charge spécialisée de pointe.
Pour en savoir plus
- www.orpha.net
- Marzano AV, Trevisan V, Lazzari R, Crosti C. Pyoderma gangrenosum: study of 21 patients and proposal of a ‘clinicotherapeutic’ classification. J Dermatolog Treat 2011 ; 22 : 254-60.
- Su WP, Davis MD, Weenig RH et al. Pyoderma gangrenosum: clinicopathologic correlation and proposed diagnostic criteria. Int J Dermatol 2004 ; 43 : 790-800.
- Vignon-Pennamen MD, Wallach D. Dermatoses neutrophiliques. EMC Dermatologie 2016 ; doi : 10.1016/S0246-0319(16)63608-7.
- Von den Driesch P. Pyoderma gangrenosum: a report of 44 cases with follow-up. Br J Dermatol 1997 ; 137 : 1000-5.

