Arthroplasties totales de hanche : évolution au cours des dernières années
La chirurgie de la hanche s’est profondément transformée ces dernières années. Cela ne concerne pas seulement l’évolution technique ou les matériaux : on assiste également à une modification du profil de nos patients. La prothèse de hanche devait jusqu’à présent répondre à un cahier des charges strict comprenant l’indolence, la stabilité et la mobilité. Maintenant, elle doit être performante sur le plan sportif pour nos patients les plus jeunes, mais aussi pour les moins jeunes qui continuent à pratiquer des activités physiques soutenues comme la randonnée, le ski, le tennis ou le golf.
Rappel historique
Sir John Charnley a popularisé le développement de la prothèse totale de hanche (PTH) à travers le monde avec son concept de « low friction arthroplasty » dans les années 1960. Cette philosophie associait un abord par trochantérotomie, une tige en chrome-cobalt polie avec un épais manteau de ciment et une bille acier de 22,2 mm de diamètre qui s’articulait dans une cupule en polyéthylène. Cette prothèse était remarquable par sa robustesse et sa longévité. Le défi était dans un premier temps d’implanter une prothèse de hanche qui puisse s’accrocher dans l’os du patient. La prothèse est ainsi fixée à l’os soit par un manteau de ciment, soit par une fixation sans ciment. Dans ce dernier cas, l’implant doit se bloquer de façon stable dans la cavité acétabulaire ou fémorale. Cette fixation primaire se poursuit par la repousse osseuse autour de l’implant, stimulée par un ostéo-inducteur, l’hydroxyapatite.
La deuxième problématique était la survie des implants. Cette survie est définie par le moment où la prothèse est changée. Les causes les plus fréquentes sont l’usure ou le descellement des implants. Le taux de survie est aujourd’hui supérieur à 95 % à 10 ans toutes prothèses confondues [1].
Prévalence et incidence
On estime actuellement la prévalence des PTH aux États-Unis à 0,83 %, soit environ 2,5 millions de personnes [2]. Toutes les projections estiment que cette demande va s’accroître de 174 % en 25 ans [3], associé à un rajeunissement significatif de l’âge des patients [2]. En effet, environ 1/3 de nos patients opérés de PTH sont en pleine activité professionnelle et ont entre 45 et 65 ans [4]. Ces données contrastent avec l’imaginaire collectif partagé par nos patients et les professionnels de santé, qui considèrent encore qu’une intervention de PTH ne peut se pratiquer qu’après 65 ans. Actuellement, l’âge n’est plus un critère de sélection chirurgicale.
PTH et sport
Il est tout à fait possible de reprendre une activité sportive après PTH. Des recommandations sont publiées régulièrement par les sociétés savantes. En réalité, ces recommandations sont issues de simples enquêtes d’opinion réalisées auprès de chirurgiens : il s’agit donc de consensus basés sur l’expérience personnelle et des attitudes de prudence [5].
Les principales raisons entravant la reprise sportive après PTH sont l’appréhension de la luxation, la peur de l’usure et le défaut de conviction du chirurgien [6].
En pratique, la majorité des patients peuvent espérer reprendre leur activité sportive au bout de 3 à 6 mois [7]. Les facteurs prédictifs du retour à un haut niveau d’activité sont de bons scores de fonctions préopératoires (score UCLA), le profil idéal étant d’être un homme jeune et sans surpoids [8].
Les tendances actuelles
Les patients opérés sont donc plus jeunes et ont des ambitions sportives importantes. Les implants sont préférentiellement des tiges et des cupules sans ciment. La voie d’abord postérieure reste la plus utilisée, mais la voie antérieure gagne du terrain. L’amélioration de la prise en charge globale périopératoire avec les protocoles de réhabilitation accélérée autorise un raccourcissement du séjour dans la structure de soins. La rééducation douce par un kinésithérapeute garde une place dans l’accompagnement du patient en postopératoire, mais les centres de rééducation sont de moins en moins utiles pour les PTH de première intention.
La survie des implants est remarquable : elle est évaluée à 95,6 % à 10 ans et à 85 % à 20 ans, toutes prothèses confondues [9]. Si on ne s’intéresse qu’aux implants céramique/ céramique chez les patients de moins de 50 ans, il n’y a aucune usure et aucune ostéolyse à 10 ans de recul [10].
Les enjeux d’aujourd’hui
Le développement de la PTH à ses débuts était intrinsèquement dépendant de l’amélioration de la fixation des implants et de la diminution de l’usure. Il s’agissait bien évidemment d’une condition indispensable qui a fait le succès de cette intervention. Aujourd’hui, la problématique est tout autre, nous recherchons la reconstruction idéale de l’articulation pour des sujets sportifs, actifs, à espérance de vie élevée. Cette reconstruction idéale fait l’objet de nombreuses controverses.
Notre philosophie
Il s’agit clairement de remettre le patient au centre de sa prise en charge. Notre métier est un art dont l’essence même est de s’adapter à la demande de nos patients [16]. Une technique chirurgicale adaptée et la personnalisation de la relation médecin/ malade sont notre moyen d’y arriver. En effet, le gain de mobilité et la suppression de la douleur sont insuffisants, et nous avons aussi un rôle majeur de conseil et d’accompagnement dans la reprise des activités professionnelles et sportives.
Privilégier la voie antérieure
Respectueuse de la musculature, la voie antérieure est notre abord privilégié. Il s’agit de la seule technique chirurgicale qui préserve l’anatomie de nos patients puisqu’aucun muscle ou tendon n’est traumatisé ou sectionné pendant la chirurgie. Par ailleurs, une méta-analyse récente de 2015 semble démontrer de meilleurs résultats sur le risque d’instabilité [17].
Choix des implants
Nous privilégions les prothèses en titane sans ciment qui permettent l’utilisation d’un couple de frottement céramique-céramique. Il s’agit actuellement du glissement qui présente le plus faible niveau d’usure dans le temps. Une technique chirurgicale précise est indispensable afin d’éviter un certain nombre de complications liées à ce type de matériau. De nos jours, le risque de casse théorique est devenu exceptionnel.
Planification 3D (Fig. 1-3)
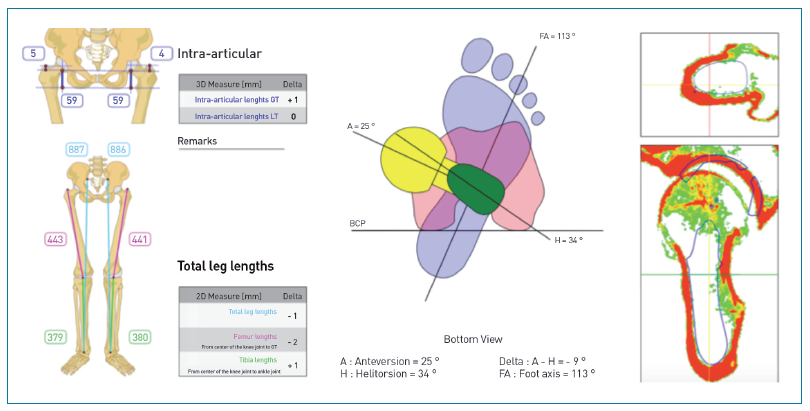
Figure 1 – Planification 3D.

Figure 2 – La prothèse de hanche sur mesure : un objet unique.
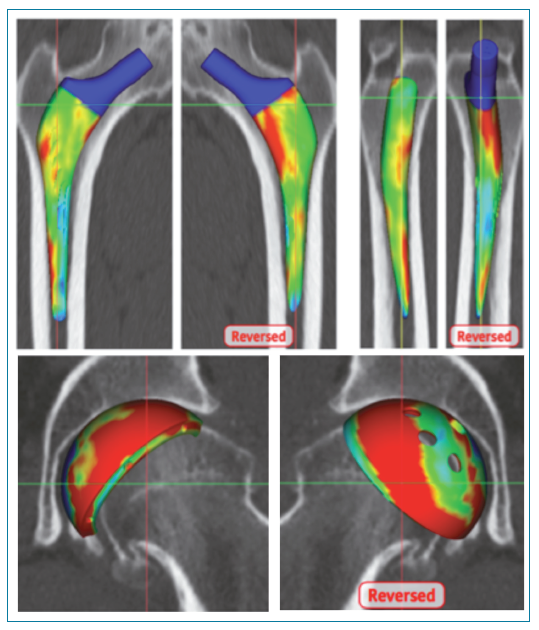
Figure 3 – Le rendu volumétrique de la prothèse sur mesure planifiée en 3D.
Préserver l’anatomie de nos patients est essentiel, mais insuffisant. Nous souhaitons également reconstruire l’anatomie articulaire de la hanche le plus fidèlement possible. Ainsi, tous nos patients bénéficient d’une analyse tridimensionnelle par un scanner selon un protocole spécial (Fig. 1). Des renseignements sur le centre de rotation de la hanche, la longueur des membres, la forme, l’orientation et la taille du cotyle et du fémur sont recueillis. Le scanner donne également des informations précises sur l’anatomie intramédullaire et la qualité osseuse. Nous planifions alors le positionnement et la taille idéale de notre prothèse en 3D. La planification précise des implants est importante, car elle conditionne le bon résultat à court terme, mais également à long terme. En effet, une modification du centre de rotation de la hanche entraîne une augmentation du risque de surcontrainte articulaire et donc d’usure théorique [18].
L’implant sur mesure, en particulier la tige fémorale, permet de reproduire la planification 3D avec un haut niveau de fiabilité. En effet, le degré de précision opératoire est élevé pour la restauration de la longueur des jambes et la remise en tension idéale des muscles. Par ailleurs, le contrôle précis de la rotation du pied n’est possible qu’avec une tige fémorale sur mesure.
Bien évidemment, cela dépend de la finesse avec laquelle le chirurgien est capable de reconstruire le centre de rotation de la hanche planifié. Les implants sur mesure sont tout à fait adaptés pour tous nos patients ayant une dysplasie acétabulaire et/ ou une dysmorphie fémorale. Cette technologie nous semble également adaptée pour les patients jeunes et sportifs, avec un enjeu sur le contrôle du risque de complications.
Conclusion
L’OMS considère que l’opération de PTH a été une des révolutions médicales du XXe siècle en diminuant le handicap à travers le monde. Aujourd’hui, la PTH doit accompagner le patient vers la performance. Une meilleure compréhension de l’anatomie articulaire et notre capacité à reconstruire avec précision l’articulation de la hanche sans endommager la puissante musculature environnante sont les clés pour atteindre cet objectif de performance. L’intervention de PTH est aujourd’hui devenue une chirurgie certes classique, mais de plus en plus technique car les attentes de nos patients ont changé.

Bibliographie
- Kandala NB, Connock M, Pulikottil-Jacob R et al. Setting benchmark revision rates for total hip replacement: analysis of registry evidence. BMJ 2015 ; 350 : h756.
- Maradit Kremers H, Larson DR, Crowson CS et al. Prevalence of Total Hip and Knee Replacement in the United States. J Bone Joint Surg Am 2015 ; 97 : 1386-97.
- Patel A, Pavlou G, Mújica-Mota RE, Toms AD. The epidemiology of revision total knee and hip arthroplasty in England and Wales: a comparative analysis with projections for the United States. A study using the National Joint Registry dataset. Bone Joint J 2015 ; 97-B : 1076-81.
- Kim S. Changes in surgical loads and economic burden of hip and knee replacements in the US: 1997-2004. Arthritis Rheum 2008 ; 59 : 481-8.
- Bradley BM, Moul SJ, Doyle F, Wilson MJ. Return to Sporting Activity After Total Hip Arthroplasty-A Survey of Members of the British Hip Society. J Arthroplasty 2017 ; 32 : 898-902.
- Ollivier M, Frey S, Parratte S et al. Pre-operative function, motivation and duration of symptoms predict sporting participation after total hip replacement. Bone Joint J 2014 ; 96-B : 1041-6.
- Cowie JG, Turnbull GS, Ker AM, Breusch SJ. Return to work and sports after total hip replacement. Arch Orthop Trauma Surg 2013 ; 133 : 695-700.
- Williams DH, Greidanus NV, Masri BA et al. Predictors of participation in sports after hip and knee arthroplasty. Clin Orthop Relat Res 2012 ; 470 : 555-61.
- Bayliss LE, Culliford D, Monk AP et al. The effect of patient age at intervention on risk of implant revision after total replacement of the hip or knee: a population-based cohort study. Lancet 2017 ; 389 : 1424-30.
- Chana R, Facek M, Tilley S et al. Ceramic-on-ceramic bearings in young patients: outcomes and activity levels at minimum ten-year follow-up. Bone Joint J 2013 ; 95-B : 1603-9.
- Palazzo C, Jourdan C, Descamps S et al. Determinants of satisfaction 1 year after total hip arthroplasty: the role of expectations fulfilment. BMC Musculoskelet Disord 2014 ; 15 : 53.
- Hagen TP, Vaughan-Sarrazin MS, Cram P. Relation between hospital orthopaedic specialisation and outcomes in patients aged 65 and older: retrospective analysis of US Medicare data. BMJ 2010 ; 340 : c165.
- Ravi B, Jenkison R, Austin PC et al. Relation between surgeon volume and risk of complications after total hip arthroplasty: propensity score matched cohort study. BMJ 2014 ; 348 : g3284.
- Birkmeyer JD, Stukel TA, Siewers AE et al. Surgeon volume and operative mortality in the United States. N Engl J Med 2003 ; 349 : 2117-27.
- Bronson WH, Lindsay D, Lajam C et al. Ethics of Provider Risk Factor Modification in Total Joint Arthroplasty. J Bone Joint Surg Am 2015 ; 97 : 1635-9.
- Jourdan C, Poiraudeau S, Descamps S et al. Comparison of patient and surgeon expectations of total hip arthroplasty. PLoS One 2012 ; 7 : e30195.
- Higgins BT, Barlow DR, Heagerty NE, Lin TJ. Anterior vs. posterior approach for total hip arthroplasty, a systematic review and metaanalysis. J Arthroplasty 2015 ; 30 : 419-34.
- Knahr K. Tribology and total hip arthroplasty implants. Orthopedics 2013 ; 36 : 854-5

