Choix de la greffe dans les reconstructions du ligament croisé antérieur
Connaître les complications et morbidités des autogreffes pour la prévention des échecs et l’orientation de la rééducation post-opératoire
Les lésions traumatiques du ligament croisé antérieur (LCA) sont fréquentes en pratique sportive. Une fois l’indication chirurgicale de reconstruction du LCA posée, la discussion se portera sur le choix de la greffe ligamentaire. Ce dossier s’intéressera ici aux autogreffes, à l’exclusion des greffes synthétiques (actuellement non utilisées) et des allogreffes (dont l’accessibilité reste difficile en pratique courante et leur utilisation très spécifique tout du moins sur le territoire français).
Introduction
Résultats des reconstructions et suites opératoires
Les résultats des reconstructions du LCA sont bons à très bons selon les études dans plus de 85 % des cas (1). Pourtant, les suites opératoires ne sont pas toujours simples et la rééducation après ce type d’intervention n’est pas un long fleuve tranquille avec une variabilité inter-individuelle non négligeable.
Cahier des charges
Le cahier des charges d’une reconstruction du ligament croisé antérieur doit répondre à plusieurs critères :
• récupération fonctionnelle globale, notamment la reprise du même sport au même niveau,
• la laxité résiduelle,
• l’instabilité résiduelle
• et le taux de rupture itérative de la greffe.
Le choix de la greffe inclura donc l’ensemble de ces critères en plus des critères liés :
• au type d’activité sportive principale,
• à l’âge,
• au sexe,
• aux antécédents traumatiques (tendinopathie, rupture tendineuse…) et chirurgicaux (ligamentoplastie itérative ou multiligamentaire).
Les différents types d’autogreffes
Il faut bien distinguer choix du type de greffe et technique chirurgicale. En effet, il n’est pas discuté dans ce dossier des types de fixation des greffes ou des techniques de greffe longue ou courte, mais de la morbidité et de la iatrogénie liée à la prise de tel ou tel greffon.
Types de greffon
Actuellement, plusieurs autogreffes sont utilisées :
• le tiers central du tendon rotulien (KJ) (Fig. 1),
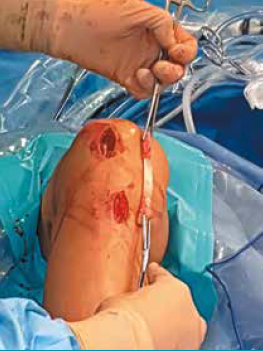
• les tendons ischio-jambiers avec greffe à quatre brins (IJ) (Fig. 2),
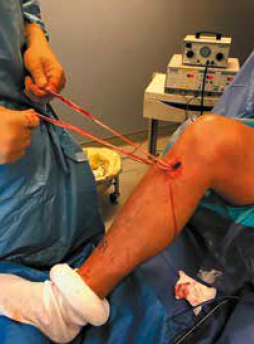
• le fascia lata renforcé au gracilis (McFL) (Fig. 3)
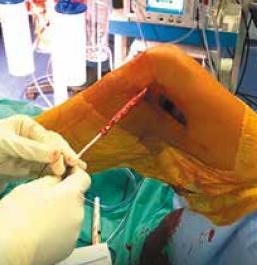
• et le tiers central du tendon quadricipital (TQ) (Fig. 4).
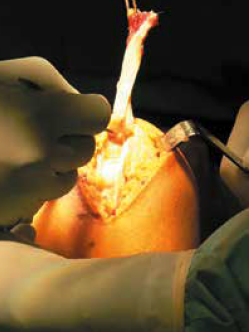
Paramètres à prendre en compte
Les études biomécaniques fondamentales permettent de définir deux notions importantes :
• la résistance maximale à la traction : c’est la force nécessaire en Newton pour rompre la greffe ;
• le module d’élasticité : c’est le point, exprimé en Newton/mm, à partir duquel la déformation de la greffe n’est plus réversible, c’est-à-dire qu’à partir de cette traction la greffe présentera un allongement résiduel sans se rompre.
Plusieurs études ont permis d’étudier ces paramètres principaux et il apparaît que l’utilisation du tendon patellaire, du tendon quadricipital et des ischio-jambiers en quatre brins induit des résistances maximales et des modules d’élasticité supérieurs à un LCA natif (2). Les études sur le fascia lata retrouvaient une moins bonne résistance à la traction, cependant, il n’a pas été fait d’évaluation avec les techniques modernes du McFL augmentant le diamètre de la greffe avec un tendon gracilis en deux brins. Ces études expérimentales sont à nuancer, car elles n’analysent pas les phénomènes d’évolution de la greffe à moyen et long termes dans du tissu vivant et notamment les phénomènes biologiques d’intégration et de transformation des greffes in vivo.
Résultats fonctionnels
L’analyse des résultats fonctionnels et des résultats sur la laxité résiduelle et le taux de rupture itérative des différents types de greffon dans la littérature est très difficile à évaluer. Beaucoup de publications sur le sujet, essentiellement lorsqu’elles sont comparatives, portent sur KJ versus IJ et bien souvent il s’agit de méta-analyses. Les évaluations des greffes de TQ et McFL sont rarement comparées à d’autres greffes (3-4). L’utilisation du tendon patellaire retrouverait de meilleurs résultats sur le contrôle de la laxité, le taux de rupture itérative et le ressaut rotatoire résiduel. En revanche, il semblerait qu’il existe moins de complications et de morbidités du site donneur avec l’utilisation des ischio-jambiers. Sur le résultat fonctionnel et la reprise du même sport au même niveau, aucune différence ne peut actuellement être mise en évidence entre les quatre types de greffon nous intéressant dans ce dossier (5-11).
Nous nous attacherons donc aux principaux problèmes posés par la prise du transplant lors des ligamentoplasties pour rupture du ligament croisé antérieur. Cette analyse nous semble fondamentale et il est impossible de s’exonérer de son évaluation dans les résultats de ces techniques de ligamentoplastie, chacun d’entre nous ayant été confronté au difficile problème d’une parfaite stabilisation de l’instabilité antérieure, malheureusement grevée par la iatrogénie de la prise du transplant.
1/ Iatrogénie de la prise du transplant au tendon patellaire (KJ) (12)
Il convient en préambule de se montrer prudent en différenciant des relations iatrogéniques certaines que sont :
• les tendinopathies rotuliennes,
• les fractures de la rotule,
• les ruptures du tendon rotulien,
• les instabilités rotuliennes,
• les syndromes neuro-tronculaires,
des relations iatrogéniques incertaines, voire indirectes, que sont :
• les douleurs antérieures fémoro-patellaires.
• les raideurs et diminutions d’amplitudes articulaires.
• la faiblesse résiduelle du système extenseur.
La hernie du tissu cellulo-graisseux de Hoffa
Une complication rare est la hernie du tissu cellulo-graisseux de Hoffa à travers la plage cicatricielle de la prise du greffon.
Prévention
Tous les auteurs s’accordent à considérer le potentiel de régénération du tendon et d’insister sur l’intérêt de faire trois ou quatre points de fermeture afin d’éviter les défects permanents et leur potentiel de complications par hernie du tissu cellulo-graisseux de Hoffa.
Les ruptures du tendon patellaire et les fractures de rotule
Les ruptures du tendon patellaire ou les fractures de rotule sont rares, puisque retrouvées dans 9 cas sur 490 dossiers d’un travail de Christen et 4 cas sur 604 dossiers d’un travail de Kartus (13). Leur fréquence est faible voire exceptionnelle, souvent inférieur à 0,01 % selon les séries.
Diagnostic
Le diagnostic est évident avec un début brutal, traumatique et une impotence complète du système extenseur. Il faut insister sur cette notion de traumatisme initial le plus souvent consécutif à un travail excessif en protocole accéléré du système extenseur, d’une descente trop rapide d’escaliers ou d’un sevrage trop rapide de l’attelle d’extension avec son corollaire de chute.
Prévention
Ceci suppose donc une attitude préventive reposant sur :
• une prise du greffon la moins agressive possible ;
• un maintien beaucoup plus long que dans les autres transplants d’une attelle d’extension jusqu’au verrouillage quadricipital dynamique ;
• une plus grande prudence vis-à-vis du système extenseur lors de la mise en jeu du protocole accéléré en se gardant de toute tentative inflationniste.
Les conséquences sur les pressions de l’articulation fémoro-patellaire
Modifications observées
Le prélèvement du tendon patellaire semble modifier les pressions fémoro-patellaires sur des études biomécaniques (14) :
• la pression augmente de 15 % au niveau de la facette latérale interne ;
• la pression augmente de 34 % au niveau de la facette latérale externe ;
• la pression diminue de 22 % à la partie médiane de la patella hormis juste à proximité du prélèvement osseux où elle augmente.
Ces résultats font donc la preuve d’une redistribution des pressions patellaires au niveau des surfaces de la patella.
Une étude radiographique retrouvait 47 % d’altération de l’articulation fémoro-patellaire (15) :
• 34 % modérée,
• 12 % moyenne,
• 1 % sévère.
Cependant, parmi les 53 % restants, 53 % considéraient leur genou comme anormal. Les résultats montraient dans cette étude une corrélation significative entre l’importance des lésions fémoro-patellaires et le raccourcissement du tendon rotulien, ce qui va dans le sens de différents travaux de la littérature considérant un seuil de tolérance de raccourcissement de 6 % au-delà duquel les répercussions mécaniques deviennent extrêmement délétères.
Échelles d’évaluation
Concernant les échelles d’évaluation, les patients indemnes de lésion radiographique fémoro-patellaire :
• étaient plus souvent satisfaits de leur opération,
• avaient moins de douleurs,
• avaient moins de gonflements
• et avaient une meilleure amplitude
que ceux avec lésion fémoro-patellaire. Il n’y avait pas de corrélation dans cette étude entre le degré d’instabilité résiduelle en arthrométrie et le syndrome rotulien, par contre l’évaluation musculaire isocinétique montrait à 60° de vitesse angulaire une diminution significative de force de 26 % chez ceux présentant des signes radiographiques versus 8 % chez ceux n’en présentant pas.
Ceci illustre un point fondamental dans l’évaluation globale des ligamentoplasties entre ce qui revient à la correction de l’instabilité sagittale et de la iatrogénie inhérente à la prise du transplant.
Les lésions neuro-tronculaires du nerf infra-patellaire
Anatomie
Cette morbidité est illustrée par un travail de Kartus et al. au cours duquel 60 dissections cadavériques ont été effectuées permettant d’étudier le nerf infra-patellaire (16). Ce nerf infra-patellaire passe 59 fois sur 60 entre le bord inférieur de la patella et le bord supérieur de la tubérosité tibiale antérieure, c’est donc dire qu’il sera sectionné par ces techniques
59 fois sur 60. De plus, le nerf infra-patellaire peut présenter une ou plusieurs branches :
• une branche 15 fois sur 60 ;
• deux branches 37 fois sur 60 ;
• trois branches 6 fois sur 60 ;
• quatre branches 1 fois sur 60.
La distance moyenne entre le bord inférieur de la patella et le nerf infra-patellaire ou son rameau supérieur était dans cette étude de 30 mm ± 27 mm (Fig. 5). La distance moyenne entre la tubérosité tibiale antérieure et le nerf infra-patellaire ou son rameau inférieur était de 27 mm (± 27 mm).
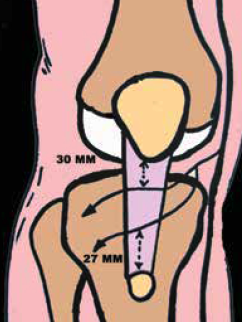
Prévention
Forts de ces éléments anatomiques, ces auteurs proposent non plus une grande incision verticale, mais deux incisions de 25 mm, l’une sous-patellaire, l’autre au-dessus de la tubérosité tibiale antérieure avec dissection première de cette TTA, le greffon étant alors tiré vers le haut, protégeant le nerf et le péri-tendon.
Les constats anatomiques de cette dissection font valoir que le nerf infra-patellaire a été lésé 13 fois sur 60, soit 22 % versus 59 fois sur 60 par technique classique et que la longueur du para-tendon intègre entre ces deux incisions était de 27 mm.
Un élément de réflexion supplémentaire repose sur les résultats d’un travail épidémiologique sur 604 ligamentoplasties montrant une corrélation significative entre douleur, déficience musculaire et hypoesthésie qui était considérée comme significative à partir de 4 cm².
Il est donc à présent recommandé de réaliser deux voies d’abord pour le prélèvement du tendon patellaire.
Les douleurs antérieures et les tendinopathies de la pointe de rotule
La morbidité sur le site donneur en lui-même favorise les douleurs antérieures et les tendinopathies de la pointe de rotule (1, 17). Notre expérience ne déroge pas des chiffres de la littérature pour considérer 40 à 70 % de problèmes, parfois mineurs et temporaires, concernant cette morbidité. Nous ne nous attarderons pas sur quelques études contradictoires, tous les travaux en IRM s’attachant néanmoins à mettre en évidence une augmentation d’épaisseur et de largeur du tendon rotulien lors des évaluations à 2 ans, pour nous attacher à l’analyse de deux études.
Chronologie de la réparation
Bernicker et al. précisent la chronologie de cette réparation. Dans cette étude, tous les patients ont bénéficié d’un suivi IRM à 3 semaines, 3 mois, 6 mois et 1 an (18).
Concernant le tendon rotulien
• Il en résulte que la largeur résiduelle du defect diminue de 61 %, mais que ce déficit ne disparaît pas complètement à 1 an.
• De même à 1 an, après diminution initiale, la largeur du tendon rotulien reprend un aspect subnormal, moins 6 %.
• La longueur du tendon rotulien diminue, elle, de 4 % et cette diminution de longueur est maximale entre le 3e et le 6e mois.
• Enfin, la section globale augmente, mais de manière non significative, plus 9 %.
Concernant les tissus mous pré-rotuliens
• 3 patients sur 12 n’ont aucune reconstruction significative.
• 5 patients sur 12 ont un tissu plus mince que le genou adjacent.
• 4 patients sur 12 ont reformé un tissu d’épaisseur normale.
Il en résulte donc, aussi bien vis-à-vis du tendon que du tissu mou pré-rotulien, une reconstruction incomplète à 1 an et qui fait vraisemblablement le lit des principaux problèmes que nous rencontrons en rééducation et lors de la reprise du terrain.
Évaluation à long terme
L’évaluation à long terme est précisée dans une publication de Kartus et al. Le principe de cette étude remarquable reposait sur une évaluation clinique, radiographique et échographique et l’imagerie par résonance magnétique nucléaire à 6 semaines, 6 mois et 26 mois (19). Ces investigations ont été complétées par une étude histologique écho-guidée sous anesthésie locale par deux prélèvements au niveau du site donneur et deux prélèvements à la périphérie non prélevée du tendon rotulien. De plus, outre une histologie classique, ce travail reposait sur une étude histochimique avec dosage du collagène 3 et des glyco-aminoglycans.
Évaluation échographique-IRM
Le premier constat échographique-IRM affine les résultats de l’étude Bernicker et al.
• Le défect tendineux diminue en taille pour disparaître complètement 3 fois sur 19 en IRM à la différence de l’échographie où il n’apparaît jamais totalement comblé.
• Dans le même temps, le couplage échographie/IRM confirme à 2 ans une augmentation de l’épaisseur et de la largeur globale du tendon prélevé par rapport au côté sain.
Évaluation histologique
L’étude histologique à 26 mois montre à tous les niveaux une augmentation de la cellularité et de la vascularisation témoignant d’un processus de réparation. Néanmoins, au niveau de la prise du greffon, la structure est altérée, reposant sur une rupture avec séparation des fibres, une fibrose et une hyalinisation du milieu, ces trois éléments étant plus ou moins intriqués entre eux.
Évaluation histochimique
Pour intégrer cette étude histochimique, il convient de se rappeler des travaux de la littérature concernant les tendinopathies chroniques d’Achille, mieux encore des tendinopathies patellaires du sauteur. Cette étude histochimique montre une augmentation de la richesse des glyco-aminoglycans et une augmentation du collagène 3. Tous ces éléments témoignent d’un processus de synthèse récent actif de cicatrisation. Dans cette étude à 26 mois, Kartus et al. ne retrouvent ni augmentation du collagène 3, ni augmentation des glyco-aminoglycans, ceci amenant ces auteurs à considérer qu’à 26 mois :
• le tissu cicatriciel a terminé sa réparation active comme en témoigne la normalité du collagène 3 et des glyco-aminoglycans ;
• ce tissu cicatriciel n’est néanmoins pas normal tant macroscopiquement qu’histologiquement, mais que ce processus est différent de ce que l’on observe dans les tendinopathies chroniques
• et ce tissu cicatriciel représente vraisemblablement l’expression d’une réparation excessive plutôt que d’un tissu anomal à 2 ans.
Ce concept histologique de réparation tissulaire excessive est en adéquation avec :
• d’une part, le constat clinique d’épaississement et parfois de rétraction des tendons rotuliens ;
• d’autre part, au constat d’imagerie, échographie et IRM montrant une augmentation d’épaisseur de la largeur du tendon à 2 ans, mais de la persistance d’un defect 16 fois sur 19 en IRM et 19 fois sur 19 en échographie.
En ce qui nous concerne, ce constat d’une non restitution ad integrum du tendon, aussi bien en imagerie qu’en histologie, nous amène à considérer avec beaucoup de circonspection la réutilisation de ce tendon cicatriciel comme nouveau site donneur.
Conclusion
Ces constats structurés sont par ailleurs, à l’évidence, le substrat de nombreuses manifestations cliniques qui grèvent cette technique par ailleurs excellente sur la stabilité que sont les tendinopathies patellaires rebelles et leur potentiel de rupture, les douleurs antérieures, la faiblesse du système extenseur, l’abaissement de la rotule par rétraction du tendon patellaire. Pour autant, un certain nombre de publications retrouve une disparition clinique des phénomènes de douleurs antérieures et de tendinopathies d’insertion à 2 ans de recul (1).
Il est bien sûr et heureusement que bon nombre de cas sont favorables, mais il faut avoir à l’esprit la iatrogénie potentielle de la prise du greffon au tendon rotulien dont nous avons vu l’éventail des manifestations et qui nécessitent en permanence de s’adapter tant dans la rééducation que dans l’accompagnement à la reprise du sport.
2/ Iatrogénie de la prise du transplant aux tendons ischio-jambiers (gracilis et semi-tendineux) (12)
Peu d’études s’intéressent spécifiquement à la morbidité du site donneur des ischio-jambiers.
Les douleurs
Il peut exister des douleurs au niveau du site donneur et de la loge musculaire des ischio-jambiers. Lors du prélèvement, il se constitue une zone fibro-cicatricielle entre le muscle et le tibia avec une proximalisation du corps musculaire. Cette modification anatomique peut être source de douleurs musculaires, de crampes résiduelles, de déficit de flexion ou de raideur des chaînes postérieures. Une rééducation adaptée permet souvent une récupération sans séquelles à long terme.
Elles peuvent être l’expression d’adhérences au niveau du site de prélèvement ou lorsque l’insertion distale est maintenue, une modification directionnelle du transplant balayant la face antéro-interne du tibia.
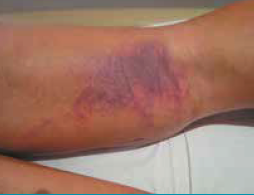
Les hématomes
Les hématomes post-opératoires immédiats (Fig. 6) ne sont pas rares et peuvent se manifester jusqu’à
15 jours après l’opération. Une simple surveillance est dans la grande majorité des cas nécessaire.
Le claquage des ischio-jambiers internes
Un des problèmes majeurs était celui des potentialités de claquage des ischio-jambiers internes, ce d’autant que, dans les sports pivots-contacts, ils sont fondamentaux car :
• ce sont les muscles de la course ;
• ce sont aussi les principaux protecteurs musculaires du ligament croisé antérieur.
Prévention
Ces potentialités de claquages itératifs existent et doivent supposer :
• une prudence extrême lors de la rééducation des ischio-jambiers les 4 à 6 premières semaines ;
• une fois passé ce délai de “cicatrisation primaire”,
√ un travail musculaire identique à celui d’une déchirure musculaire,
√ la poursuite de la physiothérapie et massages défibrosants,
√ des étirements visant à orienter la cicatrisation en respectant la non douleur,
√ un travail musculaire concentrique isométrique puis excentrique manuel à partir du troisième mois.
Les lésions neurologiques
La prise du greffon aux tendons ischio-jambiers peut, elle aussi, générer des lésions neurologiques et notamment une neurapraxie de la branche infra-rotulienne du nerf saphène interne telle que nous l’avons décrite, voire une atteinte du tronc primaire du nerf saphène interne responsable de dysesthésies et d’hypoesthésies de la face interne de jambe dans 40 à 70 % des cas (20).
Étude comparative
L’étude
Katsunori et al. ont publié une étude comparant quatre genoux de situations différentes (21) :
• genou avec ligamentoplastie et prise du greffon sur ce genou ayant présenté une rupture du LCA ;
• genou controlatéral de référence sans aucune chirurgie ;
• prise du greffon sur le genou sain controlatéral au côté blessé ;
• enfin, analyse du genou ayant bénéficié d’une ligamentoplastie sans prise du greffon puisque celle-ci a été effectuée sur le genou controlatéral.
70 patients ont été étudiés :
• 35 chirurgies avec prise du greffon sur le côté touché,
• 35 avec prise du greffon sur le côté opposé.
Tous ces genoux ont bénéficié :
• d’une évaluation subjective à 1, 3, 6, 9, 12 et 24 mois sur la douleur, la faiblesse et la reprise du sport ;
• d’une évaluation objective pré-chirurgicale à 1, 3, 6, 12 mois sur l’amplitude articulaire au goniomètre ;
• d’une évaluation isométrique aux quadriceps et aux ischio-jambiers,
• d’une évaluation isocinétique à 12 mois.
Genou sain versus genou opéré
Concernant les résultats subjectifs, genou sain versus genou opéré, il n’y a pas de différence significative à 1 an, montrant la capacité de régénération des tendons droit interne (gracilis) et demi-tendineux. Ces résultats ont été confirmés lors de plusieurs publications récentes relatives à la régénération du semi-tendineux.
Genou non opéré versus simple prise du greffon
Le genou sain après rééducation augmente sa force de 130 % de sa valeur initiale à 3 mois et de 120 % à 12 mois. Concernant le genou “prise de greffon”, il existe une diminution significative nette à 1 mois de 72 % qui s’atténue à 3 mois à 105 versus 130 %, mais il n’y a plus de différence significative à 12 mois.
L’évaluation isocinétique à 12 mois sur le pic de force, genou sain versus prise de greffon, retrouve :
• aux quadriceps, pas de différence significative
• et aux ischio-jambiers, persiste à 12 mois une discrète diminution du pic de force sur le genou prélevé.
Néanmoins, un travail plus récent de Tashiro et al. en 2003 montre que, si la force des ischio-jambiers est subtotale à 12 mois à des angulations inférieures à 70°, des déficits non négligeables (31 %) à des angles de flexion supérieurs ont été retrouvés après reconstruction par la patte d’oie.
Ligamentoplastie simple versus ligamentoplastie + prise de greffon
Pour la ligamentoplastie simple :
• on retrouve une diminution de la force isométrique aux quadriceps et aux ischio-jambiers à 1 mois d’environ un tiers qui revient à son niveau pré-opératoire à 1 an ;
• à 12 mois, l’évaluation isocinétique ne montre pas de différence significative par rapport aux valeurs de référence pré-opératoire.
Concernant les genoux ligamentoplastie + prise de greffon, la diminution de la force isométrique des ischio-jambiers à 1 mois est plus nette, mais reprend son niveau initial à 1 an.
L’évaluation isocinétique ne montre pas de différence entre les deux groupes à 12 mois qui gardent leur valeur de référence pré-opératoire, amenant les auteurs à considérer une morbidité faible de la prise de greffon au DIDT.
3/ Iatrogénie de la prise du transplant au fascia lata (McFL) (12)
Les publications de la littérature sont beaucoup plus rares concernant ce site de prélèvement. La morbidité semble moins importante supposant de différencier deux situations selon qu’il s’agit d’une iatrogénie post-opératoire immédiate ou d’une iatrogénie tardive.
Les hématomes
La morbidité immédiate de la prise du transplant au fascia lata est dominée par les potentialités d’hématomes. Ces hématomes sont quasi constants, d’importance variable, peuvent amener à une rare évacuation chirurgicale (2 à 5 %) et ne remettent pas en cause le pronostic ultérieur.
Prévention
Ceci suppose en corollaire un certain nombre de mesures post-opératoires que sont :
• le drainage et la surveillance des redons ;
• la mise en place de bandes de contention associées à la cryothérapie et posture déclive.
L’hypoperfusion du quadriceps
L’hypoperfusion du quadriceps par une fermeture trop tendue du fascia lata et une compression possible des corps musculaires est possible.
Prévention
Cette complication est évitée par l’ouverture du septum postérieur permettant de limiter les pressions de la loge quadricipital et de créer un syndrome de loge expérimental.
L’hyperpression latérale de l’articulation fémoro-patellaire
Prévention
Plus tardivement, il peut exister une hyperpression latérale de l’articulation fémoro-patellaire qui peut être anticipée par une ouverture de l’aileron latéral selon les équipes.
La hernie musculaire du vaste latéral
L’apparition d’une hernie musculaire du vaste latéral par une mauvaise cicatrisation du fascia lata peut nécessiter une reprise chirurgicale soit pour élargissement de la hernie afin d’éviter toute douleur à type de “hernie musculaire étranglée” (avec pour conséquence esthétique une tuméfaction latérale de la cuisse), soit par retente du fascia lata par fermeture directe.
Les problèmes esthétiques posés par la cicatrice sur la face externe de la cuisse (Fig. 7)
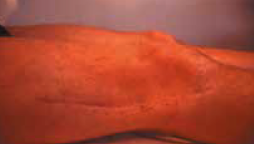
Les publications concernant l’évaluation esthétique, qu’il est tout à fait licite de prendre en compte, notamment chez une femme jeune, sont inexistantes en chirurgie orthopédique et nous avons repris pour l’illustrer une publication de 1997 du British Journal of Ophtamology (22). Pourquoi une publication ophtalmologique ? Parce que le principal transplant utilisé dans la chirurgie du ptosis est justement le fascia lata selon une bandelette d’environ 1,5 cm de large sur 12 à 15 cm de long prise 3 à 4 cm au-dessus du genou correspondant globalement au plan cicatriciel nécessaire en chirurgie orthopédique. Ces auteurs ont évalué les complications de la prise du greffon par :
• une évaluation fonctionnelle notamment des douleurs à la marche ;
• une évaluation de la cicatrice et notamment de son implication esthétique.
Douleurs à la marche
Concernant les douleurs à la marche, 67 % des patients font référence sur une durée très courte,
6 jours environ avec des extrêmes de 1 à 30 jours et une différence significative entre enfants et adultes, ces derniers ayant un temps de récupération plus long.
C’est donc dire la très faible implication fonctionnelle de la prise du greffon, isolée du geste de ligamentoplastie et ce, dans des délais très courts. À long terme, aucune douleur ni boiterie ne sont retrouvées.
Cicatrice
Concernant la cicatrice, sur l’évaluation à 20 mois, elle était considérée comme disgracieuse chez 38 % des patients, mais tous considéraient le problème comme mineur et ce, probablement relativement au problème que leur posait leur ptosis initialement.
Rééducation
Pour les rééducateurs fonctionnels et les kinésithérapeutes, les implications de la prise du greffon au fascia lata dans la plastie mixte intra et extra-articulaire sont :
• une surveillance les 10 premiers jours compte tenu du risque d’hématome ;
• par la suite, aucune restriction dans la mise en jeu du système extenseur du système fléchisseur car ces deux appareils sont conservés avec, comme toujours lors de la rééducation pour ligamentoplastie, travail quadricipital en chaîne fermée, travail des ischio-jambiers en chaîne ouverte et en chaîne fermée, cette rééducation ne posant quasiment jamais de problème.
4/ Iatrogénie de la prise du transplant au tendon quadricipital (TQ)
Les études sur la iatrogénie du tendon quadricipital sont quasi inexistantes. Le taux global de morbidité du site donneur est de 3 % d’après Mulford et al. Dans une méta-analyse, il est retrouvé des fractures de rotules d’incidence rarissime. Par ailleurs, on retrouve plus classiquement des douleurs antérieures sur la cicatrice de prélèvements avec des adhérences cicatricielles, des crépitements fémoro-patellaires. Il est retrouvé une perte de force musculaire quadricipitale le plus souvent transitoire mais qui peut parfois durer 1 à 2 ans après l’intervention (23).
Conclusion
Sous un angle original, ce dossier permet de repréciser que l’utilisation d’une autogreffe pour la reconstruction du LCA n’est pas sans conséquences.
L’importance de la rééducation
Il est évident qu’une partie de cette iatrogénie est conditionnée par la qualité de la rééducation qui fait suite à cette chirurgie de l’instabilité antéro-externe et qu’à chaque prise de greffon correspond une technique de rééducation très différenciée et qu’une partie de la iatrogénie peut être la résultante d’une rééducation “mal conduite”.
La personnalisation de la chirurgie
À la lumière de cet exposé, il apparaît qu’il n’existe aucune greffe idéale. Le choix ne doit pas se limiter à la connaissance de la iatrogénie, mais doit se faire en fonction d’un certain nombre de principes indispensables à l’optimisation des résultats.
La chirurgie du ligament croisé antérieur doit être de plus en plus personnalisée et “à la carte” pour minimiser les risques et améliorer les résultats. Ce choix doit être pris en fonction de plusieurs critères que sont l’âge, le sexe, l’importance de la laxité et du ressaut rotatoire, du type de sport pratiqué régulièrement, de la présence ou non de lésions associées méniscales ou ligamentaires périphériques. La chirurgie dogmatique est révolue, devant laisser la place à une chirurgie d’expertise pouvant passer d’un greffon à l’autre sans problèmes techniques particuliers.
L’avenir
Ces considérations concernent les autogreffes devant répondre à un compromis, mais probablement que les progrès technologiques et dans l’ingénierie tissulaire répondront à ce choix parfois cornélien en proposant :
• soit des tissus synthétiques de nouvelle génération permettant le remplacement du LCA,
• soit la production de cellules souches ligamentaires qui pourraient au sein d’une matrice de régénération reconstituer un LCA natif…
Bibliographie
1. Rousseau R, Labruyere C, Kajetanek C et al. Complications after anterior cruciate ligament reconstruction and their relation to the type of graft: a prospective study of 958 cases. Am J Sports Med 2019 ;
47 : 2543-9.
2. Noyes FR, Butler DL, Grood ES et al. Biomechanical analysis of human ligament grafts used in knee-ligament repairs and reconstructions. JBJS 1984 ; 66 : 344-52.
3. Horteur C, Cavalié G, Gaulin B et al. Saphenous nerve injury after anterior cruciate ligament reconstruction: Reduced numbness area after ligamentoplasty using quadriceps tendon compared with hamstring tendon. Knee 2020 ; 27 : 1151-7.
4. Chivot M, Pioger C, Cognault J et al. Every layer of quadriceps tendon’s central and medial portion offers similar tensile properties than Hamstrings or Ilio-Tibial Band Grafts. J Exp Orthop 2020 ; 7 : 50.
5. Lewis PB, Prameswaran AD, Rue JPH, Bernard RB. Systematic review of single-bundle anterior cruciate ligament reconstruction outcomes: a baseline assessment for consideration of double-bundle techniques. Am J Sports Med 2008 ;36 : 2028-36.
6. Barenius B, Nordlander M, Ponzer S et al. Quality of life and clinical outcome after anterior cruciate ligament reconstruction using patellar tendon graft or quadrupled semitendinosus graft: an 8-year follow-up of a randomized controlled trial. Am J Sports Med 2010 ; 38 : 1533-41.
7. Biau DJ, Katsahian S, Kartus J et al. Patellar tendon versus hamstring tendon autografts for reconstructing the anterior cruciate ligament: a meta-analysis based on individual patient data. Am J Sports Med 2009 ; 37 : 2470-8.
8. Mohtadi NG, Chan DS, Dainty KN, Whelan DB. Patellar tendon versushamstring tendon autograft for anterior cruciate ligament rupture inadults. Cochrane Database Syst Rev. 2011 ; 9 : CD005960.
9. Xie X, Liu X, Chen Z et al. A meta-analysis of bone-patellar tendon-bone autograft versus four-strand hamstring tendonautograft for anterior cruciate ligament reconstruction. Knee 2015 ; 22 : 100-10.
10. Schuette HB, Kraeutler MJ, Houck DA, McCarty EC. Bone-patellar tendon-bone versus hamstring tendon autografts for primary anterior cruciate ligament reconstruction: a systematic review of overlapping meta-analyses. Orthop J Sports Med 2017 ; 5 : 2325967117736484.
11. Samuelsen BT, Webster KE, Johnson NR et al. Hamstring autograft versus patellar tendon autograft for ACL reconstruction: is there a difference in graft failure rate? a meta-analysis of 47,613 patients. Clin Orthop Relat Res 2017 ; 475 : 2459-68.
12. Fichez O. Les plasties ligamentaires. Complications et morbidités selon la technique utilisée. In: Jaeger JH. Ligamentosplastie du LCA : Mc Intosh FL versus KJ et DIDT. Paris : Sauramps médical, 2020 :109-15.
13. Kartus J, Magnusson L, Stener S et al. Complications following arthroscopic anterior cruciate ligament reconstruction. A 2-5 years follow-up of 604 patients with special emphasis on anterior knee pain. Knee Surg Sports Traumatol Arthrosc 1999 ; 7 : 2-8.
14. Steen H, Tseng KF, Goldstein SA, Carpenter JE. Harvest of patellar tendon (bone-tendon-bone) autograft for ACL reconstruction significantly alters surface strain in the human patella. J Biomech Eng 1999 ; 121 : 229-33.
15. Jarvela T, Paakikala P, Jarvimen M. The incidence of patella femoral osteoarthritis and associated finidings 7 years after anterior cruciate ligament reconstruction with a bone-patellar tendon-bone autograft. Am J Sports Med 1999 ; 7 : 2-8.
16. Kartus J, Ejerhed L, Eriksson BI et al. The localization of the infra-patellar nerves in the anterior knee region with special emphasis on central third patellar tendon harvest: a dissection study cadaver and amputated specimens. J Arthrosc Relat Surg 1999 ; 15 : 577-86.
17. Mastrokalos D, Springer J, Siebold R, Paessler H. Donor site morbidity and return to the preinjury activity level after anterior cruciate ligament reconstruction using ipsilateral and controlateral patellar tendon autograft: a retroscpective, nonrandomized study. Am J Sports Med 2005 ; 33 : 85-93.
18. Bernicker JP. Patellar tendon defect during the first year anterior cruciate ligament reconstruction: appearence on serial magnetic resonance imaging. J Arthrosc Relat Surg 1998 ; 14 : 804-9.
20. Ochai S, Hagino T, Senga S et al Injury to infrapatellar brach of saphenous nerve in anterior cruciate ligament reconstruction using vertical skin incision for hamstring harvesting: risk and the influence of treatment outcome. J Orthop Surg Res 2017 ; 12 : 101.
21. Yasuda K, Tsujino J, Ohkoshi Y et al. Graft site morbidity with antegenous semitendinosus and gracilis tendon. Am J Sports Med 1995 ; 23 : 706-14.
22. Wheatoroft SM, Vardy SJ, Tyers AC. Complication of fascia lata harvesting for ptosis surgery. Brit J Ophtalm 1997 ; 81 : 518-83.
23. Mulford JS, Hutchinson SE, Hang JR. Outcomes for primary anterior cruciate reconstruction with the quadriceps autograft: a systematic review. Knee Surg Sports Traumatol Arthrosc 2013 ; 21 : 1882-8.

