La pathologie prépatellaire, des problématiques diverses
Lorsqu’un patient se présente pour « un problème de genou », d’emblée le clinicien met en place son arbre diagnostique. Ligaments, ménisques, cartilage, tendons sont les thèmes essentiels. Il ne faudrait cependant pas oublier la pathologie des surfaces de glissement situées en avant de la rotule. Celle-ci est riche et sans doute trop méconnue. Un coup de projecteur n’est pas inutile.
Anatomie des tissus mous prépatellaires
Une structure trilaminaire
Une étude très complète de Scott en 2003 portant sur 61 genoux de cadavres a montré qu’il existait une structure trilaminaire du tissu fibreux prérotulien dans plus de 90 % des cas des genoux examinés (Fig. 1).
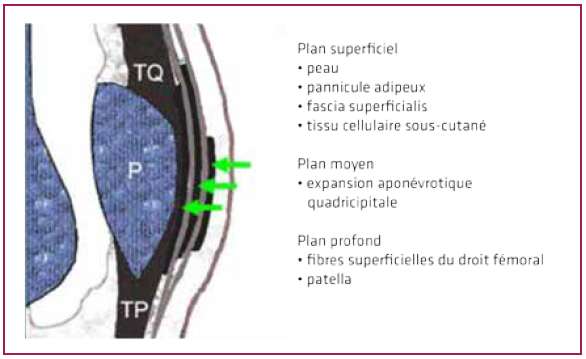
Figure 1 – Bourses prépatellaires.
La couche superficielle
La couche superficielle met en évidence une continuité des fibres du droit antérieur qui s’attache directement sur la partie antérieure de la rotule. Cette couche superficielle du fascia est peu épaisse avec une orientation des fibres transversales le long de l’axe de la rotule. Le terme de fascia a été utilisé par Reider et celui de couches arciformes par Terry.
La couche intermédiaire
Une incision longitudinale des fibres transverses de la couche superficielle permet de séparer facilement des structures profondes de la partie antérieure de la rotule. Cette incision révèle une couche d’aponévrose intermédiaire avec davantage d’orientation des fibres de manière oblique en relation avec les fibres transverses du fascia superficiel. Lorsqu’elle existe, cette structure, le plus souvent présente, est plus épaisse que la structure sus-jacente. On y retrouve des fibres de l’expansion du vaste externe et du vaste interne, de même que les fibres les plus superficielles correspondent à celles du droit antérieur.
Cette couche intermédiaire est facilement séparée de la couche profonde des fibres du droit antérieur jusqu’à la partie interne latérale et proximale de la rotule où il devient impossible de les séparer sans une importante dissection. Une incision de cette aponévrose intermédiaire révèle l’orientation profonde longitudinale des fibres du droit antérieur sur la rotule.
La couche antérieure
La troisième est la plus profonde couche de fibres tissulaires. Elle est formée par la continuité des fibres profondes du droit antérieur. Les fibres longitudinales du droit antérieur qui forment cette couche antérieure sont notées comme adhérentes de façon dense à l’os, sans la possibilité d’un espace entre les fibres du droit antérieur et l’os.
Les bourses prépatellaires
Les anatomistes estiment que, dans la majorité des genoux disséqués, il existe trois espaces potentiels antérieurs de la rotule qui peuvent avoir le terme de bourse :
- un premier espace situé entre la peau et le fascia superficiel,
- un deuxième espace entre la couche superficielle et la couche intermédiaire,
- un troisième espace entre la couche intermédiaire et la couche profonde comme cela a été décrit dans un atlas anatomique de H. Hollinshead en 1969.
On décrit la possibilité de trois bourses prépatellaires qui sont des espaces de glissement et qui ne contiennent pas de synoviocytes.
Une bourse prépatellaire superficielle (subcutanée)
Elle est présente dans 80 % des cas selon Testut. Elle communique avec la bourse moyenne dans environ 25 % des cas. Elle se trouve située dans un dédoublement du fascia superficialis. Elle est à peine visible, qu’il s’agisse d’une imagerie d’échographie ou de résonance magnétique. Elle est très fine (moins de 2 mm).
Une bourse prépatellaire moyenne (subfasciale)
Elle est présente dans près de 93 % des cas. Elle communique avec la bourse superficielle, mais rarement avec la profonde. C’est la plus volumineuse et la mieux délimitée des trois bourses. Elle est située entre le fascia superficialis et l’expansion quadricipitale.
Une bourse prépatellaire profonde (subtendineuse, subaponévrotique)
Elle est présente dans 70 à 80 % des cas. Sa localisation est plus difficile. Elle est située entre l’expansion quadricipitale et la face antérieure de la rotule recouverte par les fibres superficielles du droit fémoral. Elle semble bien délimitée.
La graisse antérieure du genou
La graisse antérieure du genou se décompose principalement en trois “matelas” graisseux.
- En premier lieu, intracapsulaires, mais extra-synoviaux : le corps adipeux infrapatellaire (CAiP ou graisse de Hoffa) et la graisse préfémorale ou supratrochléenne.
- En second lieu, la graisse sous-cutanée antérieure. Elle est d’épaisseur très variable. Elle supporte, immédiatement après la peau, les forces de compression et de cisaillement lors de différentes circonstances : chute sur les genoux, choc tangentiel, position à genoux prolongée (bricoleurs, carreleurs). Elle présente des pathologies et des problématiques très différentes de la graisse profonde (Hoffa, graisse suprapatellaire). Cette graisse superficielle antérieure montre la présence de multiples petites cloisons fibreuses dont le rôle est de renforcer sa cohésion avec la peau et de répartir les contraintes mécaniques. À proximité de ces cloisons fibreuses existent des petits éléments vasculaires et lymphatiques impossibles à mettre en évidence en imagerie à l’état physiologique.
Le syndrome de Morel-Lavallée
Il porte le nom d’un célèbre chirurgien du XIXe siècle, Victor-Auguste- François Morel-Lavallée qui a laissé derrière lui de nombreuses publications chirurgicales, particulièrement dans le domaine traumatologique (encadré 1) .

Description
Le syndrome de Morel-Lavallée est une collection séreuse située entre la graisse hypodermique et le plan des fascias sous-jacent à la suite d’un clivage d’origine traumatique. La localisation rotulienne est la plus fréquente, mais elle existe également au niveau du coude, de la face externe de la hanche et du dos. Le cisaillement des fascias et des petits éléments fibreux de cohésion de la graisse associée à l’interruption des plexus vasculaires hypodermiques entraîne la création d’une cavité virtuelle qui se remplit progressivement de sang ou de lymphe et qui peut contenir des lobules graisseux disséqués. Le volume peut être impressionnant. Une réaction inflammatoire secondaire peut aboutir à la formation d’une pseudo-capsule. À la phase constituée, la lésion se présente souvent comme une masse indolore compressible (Fig. 2).
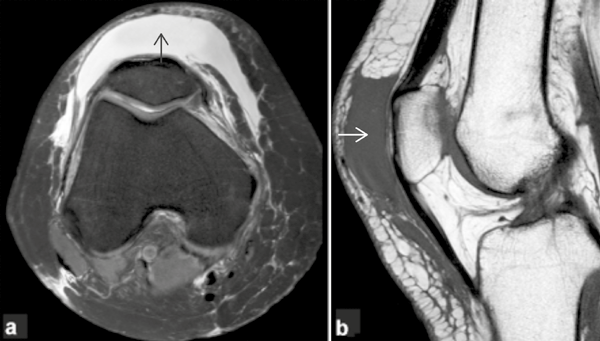
Figure 2 – Épanchement de Morel-Lavallée post-traumatique.
Diagnostic, évolution et traitement
L’échographie fait facilement le diagnostic. Au stade aigu, il s’agit d’un véritable hématome qui éventuellement à la phase chronique peut être entouré d’une coque fibreuse. Parfois, cette poche disparaît spontanément, mais souvent des ponctions sont nécessaires. Bien souvent, il persiste pendant de longues semaines une granulation sous-cutanée avec une douleur qui gêne ou empêche la position à genoux.
La résonance magnétique visualise parfaitement cet épanchement, elle n’est pas plus performante que l’échographie qui doit être préférée. L’épanchement peut persister des mois et récidiver malgré des ponctions itératives.
L’hygroma ou la pseudo-bursite
Description et diagnostic
Des adaptations au niveau des zones d’appui
La position à genoux est quasiment incontournable pour certains métiers tels que les poseurs de parquet, les carreleurs ou lors de certains sports tels que le judo ou la lutte, dans certaines activités de loisirs, bricolage ou jardinage. Des adaptations vont se produire au niveau des zones d’appui avec un épaississement de la peau réalisant une callosité plus ou moins protectrice. Au niveau de la graisse prépatellaire, on constate des modifications dans un premier temps non symptomatiques avec en résonance magnétique un œdème très fréquent. En échographie, très précisément décrite par Lapegue, on peut noter un épaississement hyper-échogène et une perte de l’architecture normale de la graisse située entre la peau et le tendon patellaire avec différenciation entre les cloisons hyperéchogènes et le contenu graisseux moins échogène.
Pré-hygroma
À un stade plus avancé (pré-hygroma), cette différenciation échographique note un aspect épaissi et un infiltrat hypoéchogène des cloisons fibreuses au sein de cette graisse superficielle. Les lobules graisseux sont plus volumineux, moins élastiques, et il existe une altération des cloisons fibreuses et des plexus vasculaires avec un exsudat entre les lobules graisseux.
Hygroma
Le stade ultime aboutit à la formation d’un hygroma. La rupture complète des cloisons fibreuses entraîne une véritable dissection de la graisse à l’endroit où les forces de cisaillement sont les plus importantes. La suffusion de lymphe et de sang entre les lobules ainsi disséqués entraîne la formation d’une collection mal limitée. On peut observer, non pas un plan de clivage net comme dans le syndrome de Morel-Lavallée, mais plusieurs plans de clivage globalement parallèles, délimitant des feuillets graisseux disséqués. Les lobules graisseux peuvent flotter nombreux dans la collection. L’échographie est un excellent moyen d’en faire le diagnostic (Fig. 3 et 4).
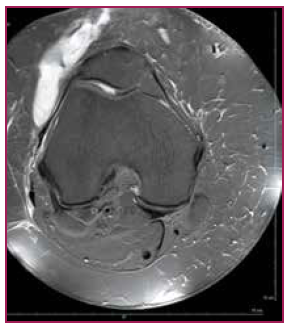
Figure 3 – Hygroma
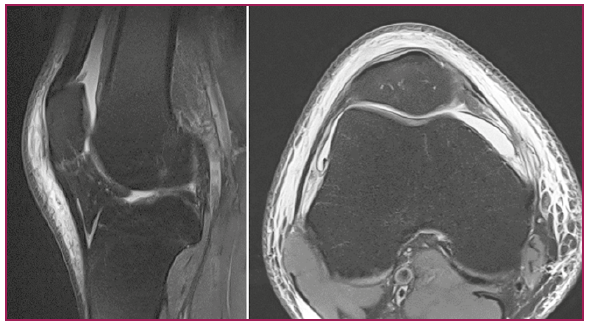
Figure 4 – Modification de la graisse prérotulienne post-traumatique. Coupe sagittale T2,
coupe axiale T2.
Phase aiguë
Au stade aigu, on observe fréquemment une collection souvent étendue, anéchogène, très facilement compressible par la sonde, le seul poids de la sonde ou de la main de l’opérateur pouvant chasser le liquide. Il n’est pas exceptionnel de retrouver dans cette collection des petits débris tissulaires, voire des lobules graisseux libres ou partiellement détachés, ou de constater un niveau liquide.
Phase chronique
À la phase chronique, la collection est souvent entourée d’une coque fibreuse bien individualisable. Parfois, en cas de disparition de la collection, cette zone fibreuse ou même simplement le plan de clivage interne de la graisse peut persister. Seules des manœuvres dynamiques vont pouvoir objectiver le mouvement des couches graisseuses de part et d’autre de ce plan de clivage. Cette sémiologie échographique peut être transposée en IRM.
Autres étiologies
D’autres étiologies dans la formation de ces hygromas sont également retrouvées, notamment des bursopathies microcristallines, infectieuses (tuberculose) ou inflammatoires. La goutte est la première cause. L’hygroma peut parfois être le révélateur de la maladie. Il existe également des bursites calcifiantes contenant de l’apatite, comme dans la sclérodermie (CREST syndrome).
Le traitement médical
La ponction
Le traitement médical n’est pas parfaitement codifié. La plupart des auteurs préconisent la ponction de cette poche qui recueille habituellement au départ un liquide franchement hématique qui, secondairement, évolue davantage vers un liquide séreux. Dans la plupart des cas, il existe une récidive.
Éviter la récidive et la surinfection
C’est pourquoi plusieurs techniques sont préconisées pour limiter le risque. À la suite de la ponction, une contention doit être instituée souvent associée à un repos articulaire par une éventuelle attelle en extension. On peut également effectuer au niveau cutané des pansements alcoolisés avec de l’alcool iodé à 2 %. Il faut cependant rester méfiant quant à la tolérance cutanée. Par ailleurs, des produits sclérosants injectés dans la poche peuvent être utilisés. L’injection d’un produit à base de corticoïdes retard est également largement utilisée. Le risque majeur des ponctions, et encore davantage si l’on utilise les corticoïdes, est la surinfection. Néanmoins, il faut tenter de ne pas chroniciser l’épanchement et ainsi éviter la formation d’une capsule autour de l’épanchement qui sera alors très difficile à traiter médicalement.
La surinfection est bien connue, même en dehors de toute ponction. Certaines activités, notamment sportives telles que la lutte et la pratique de la voile à haut niveau, sont réputées pour des risques élevés de surinfection très habituellement au staphylocoque.
Le traitement chirurgical
Par incision et excision de la poche capitonnage
Jusqu’aux années 2000, les différents chirurgiens amenés à s’occuper de ce type de pathologie utilisent des techniques par incision et excision de la poche capitonnage. Certains, tel Knight en 1986, décrivent des techniques percutanées pour éviter une intervention chirurgicale, mais avec des hospitalisations longues, de plus d’une semaine.
Par technique endoscopique
Il faut attendre les années 1990 pour que certains auteurs pensent à utiliser la technique endoscopique pour essayer de résoudre ce problème, c’est le mérite de Kerr et Carpenter (encadré 2) .

En 1998, Kalund décrit la résection endoscopique de l’hygroma prérotulien septique sur quatre patients. Il ne laisse pas de Redon aspiratif en postopératoire et, avec une antibiothérapie associée adaptée, ils ont obtenu de bons résultats à 3 mois dans les quatre cas. Depuis, les techniques endoscopiques se sont largement développées et améliorées. Pour certains comme Nickerson en 2014, une évacuation de plus de 50 ml doit pousser plus rapidement à un traitement chirurgical, du fait du fort taux de récidive à plus de 80 %. Pour Penaud, un traitement chirurgical « peu douloureux et n’imposant pas de rançon cicatricielle importante » consiste en une dermabrasion (sclérothérapie) de la capsule à l’alcool absolu. Le principe est de créer une irritation de la capsule et ainsi de générer un processus inflammatoire important permettant d’aboutir dans la majorité des cas à une fibrose (cicatrisation) complète de l’épanchement.
Compte tenu des avancées, on peut estimer que le traitement de cette pathologie continuera d’évoluer vers une simplification sans nécessité de chirurgie invasive.
La tumeur glomique
Description
Il s’agit d’un réseau anastomotique entre une artériole et une veinule réalisant un shunt dévolu à la thermorégulation. Elle représente moins de 2 % des tumeurs des parties molles et 75 % se situent au niveau des doigts. La série de Schiefer retrouve six cas au niveau du genou sur les 56 cas de sa série.
Diagnostic et traitement
La clinique est relativement typique avec une douleur focale intense paroxystique majorée à la pression sur une zone gâchette. Le diagnostic est souvent retardé jusqu’à 7 ans. L’échographie est un excellent moyen de diagnostic. La résection chirurgicale règle en général le problème.
Le syndrome de friction prépatellaire
Description
C’est une cause commune de douleurs du genou chez les cyclistes professionnels. De Bernardo montre que 62,7 % de tous les cyclistes présentent des douleurs causées par un syndrome de surutilisation et 32 % concernent le genou.
Silberman note que, lors de chutes, le genou et l’épaule sont les principaux sites touchés. Clarsen indique par ailleurs qu’après les douleurs lombaires, la douleur antérieure du genou est la deuxième cause la plus importante chez les cyclistes professionnels.
Le terme de douleur antérieure du genou est un syndrome clinique, non un diagnostic. Traditionnellement, le cartilage et l’os sous-chondral de la fémoro-patellaire sont considérés comme les éléments essentiels des douleurs du genou dans la population générale.
Cette pathologie fémoro-patellaire a été montrée bien souvent associée à un déficit de volume et de force du muscle quadriceps. Cependant, chez les cyclistes, ce muscle quadriceps est particulièrement développé. Les douleurs de la partie antérieure du genou chez ces cyclistes ne correspondent pas au classique syndrome fémoropatellaire. Cela suggère qu’il existe une autre entité de douleurs de la partie antérieure du genou chez les cyclistes professionnels.
En 2003, Dye fut le premier à décrire le complexe anatomique des tissus mous situés en avant de la rotule. La présence de trois bourses en avant de la rotule confirme l’importante exposition à la friction.
Causes
Les cyclistes de haut niveau effectuent un acte répétitif qui entraîne des phénomènes de friction. En 4 heures de vélo, un cycliste à la cadence de 85 tours/min aura réalisé 20 400 tours de pédale.
Un alignement dysplasique de la rotule et un équipement inadapté peuvent faciliter le déclenchement d’une pathologie. Lorsqu’il n’y a pas de traumatisme, la douleur débute habituellement après un long entraînement, à la suite d’un stage… L’augmentation de la vitesse de rotation peut être un phénomène aggravant. La douleur est augmentée lorsque le cycliste pédale vite, elle diminue lorsqu’il réduit la cadence en dehors de toute modification de la puissance. Le fait de monter en danseuse, paradoxalement, diminue souvent la douleur, car il existe une flexion de genou moins accentuée et une cadence moins rapide. À noter que lors des syndromes fémoropatellaires, c’est le contraire qui se produit.
Chez les cyclistes, la douleur apparaît souvent en hiver, parce que l’athlète porte alors des pantalons pour se protéger du froid et que cela augmente la pression sur l’avant du genou. Les genouillères peuvent être également un facteur d’aggravation.
Diagnostic
La palpation retrouve une zone de souffrance localisée avec parfois une irrégularité. La localisation la plus fréquente est située au niveau de la partie supéro-interne de la rotule. En dehors des efforts, la douleur peut être totalement absente. Le test anesthésique est utile. L’échographie est le gold standard. Elle permet de retrouver une zone de défect également visible sur une résonance magnétique.
Traitement
Le traitement est uniquement chirurgical et consiste à réséquer la zone pathologique qui retrouve un défect au niveau des tissus prépatellaires. Habituellement, la couche profonde est intacte, mais il existe une hyperémie et une néovascularisation.
La rééducation consiste immédiatement en un travail du quadriceps avec des techniques d’électrostimulation et des mobilisations actives et passives du genou qui sont débutées rapidement. La série de Claes regroupe 29 patients cyclistes de haut niveau. Tous les patients ont été guéris après l’intervention et le retour à la pratique sportive s’est effectué dans un délai de 3 mois au même niveau.
La pathologie traumatique prépatellaire avec douleurs de type neurologique
Description
Les chocs directs de la face antérieure du genou sont fréquents. Une série de 14 patients d’Ikpeme âgés de 17 à 60 ans évoque un traumatisme direct frontal au niveau du genou. La douleur est souvent importante lors du traumatisme avec parfois un gonflement initial. Secondairement, les patients décrivent des douleurs de type brûlure profonde situées en avant de la rotule. Il existe parfois un retentissement fonctionnel avec des difficultés pour se baisser ou pour monter les escaliers. De façon systématique, la position à genoux est insupportable. Les radiographies sont normales ainsi que l’arthrographie et l’arthroscopie.
Diagnostic et traitement
La plus fréquente des anomalies est une douleur localisée au milieu du bord externe de la rotule, mais d’autres localisations sont possibles. La palpation est améliorée par l’utilisation d’un objet dur. Une injection de 2 ml d’anesthésique et de 40 mg de corticoïdes dans la zone douloureuse repérée au préalable apporte une indolence temporaire qui signe ainsi le diagnostic. L’amélioration a été constante. Cependant, les récidives ont été nombreuses et une intervention chirurgicale a été nécessaire. Celle-ci a consisté en l’excision de la bourse de formation neurovasculaire contenant les branches antérieures de division du nerf cutané latéral de la cuisse dans un certain nombre de cas.
Les examens histologiques ont mis en évidence un épaississement de la bourse prépatellaire avec une prolifération synoviale et une exsudation de fibrine. On a noté également une prolifération de capillaires et de nerfs engainés dans la fibrose que l’on peut rapprocher d’une maladie de Morton. Il y avait aussi une fibrose relativement généralisée et du tissu fibreux et adipeux, mais pas de signe inflammatoire.
Les résultats chirurgicaux sont bons. Les patients traités chirurgicalement étaient capables à nouveau de se mettre à genoux après une période de protection pendant 5 à 8 semaines, la plus longue période par rapport à l’intervention était 3 ans. La durée d’évolution est variable, mais souvent longue avant un diagnostic correct de 6 mois à 13 ans avec des errements diagnostiques nombreux.
Il faut différencier cette douleur traumatique d’une névralgie infrapatellaire. Il s’agit à ce moment d’une souffrance du nerf saphène.
La pathologie du nerf saphène interne
Description et évolution
Le nerf saphène provient d’une division du nerf fémoral et quitte le canal de l’adducteur entre les tendons du gracilis et du demi-tendineux. Ensuite, il se divise en une branche principale, le nerf saphène, qui continue vers la cheville et la branche infrapatellaire (Fig. 5).

Figure 5 – Nerf saphène interne et ses trois branches terminales.
Celle-ci traverse le genou proche de la rotule et se divise en trois branches avant de rejoindre la branche antérieure du nerf cutané externe de la cuisse, le nerf cutané intermédiaire de la cuisse et la branche antérieure du nerf cutané interne de la cuisse qui forme ce que l’on appelle le plexus prépatellaire.
Un certain nombre d’auteurs, tel Kerver, souligne la grande variabilité d’émergence de la branche infrapatellaire du nerf saphène. Dans la majorité des cas, près de 70 %, le nerf émerge près du bord antérieur du sartorius entre la face interne de la rotule et le tronc du nerf. Dans 65 % des cas, la division du tronc du nerf est située entre la pointe de la rotule et la tubérosité tibiale antérieure. Une seule branche est observée dans 40 % des cas (Kalthur).
Les auteurs ont décrit des zones appelées « the soft point », où les risques étaient limités pour effectuer d’éventuelle incision chirurgicale.
La pathologie en rapport avec le nerf saphène interne a été largement décrite. Il s’agit le plus souvent de cas en rapport avec une chirurgie : prothèse du genou, arthroscopie, traitement d’un hygroma… La durée de l’évolution est longue et peut aller jusqu’à 10 ans.
Diagnostic et traitement
Cliniquement, il est essentiel de retrouver l’origine de la douleur, de vérifier l’absence de cicatrice et de rechercher un signe de Tinel ou une hypoesthésie. Le test anesthésique peut être très utile. Le traitement médical débute toujours par une infiltration loco dolenti de corticoïdes. En cas d’échec, une chirurgie à type de neurolyse est recommandée.
Compression de la branche infrapatellaire du nerf saphène
Description
La compression de la branche infrapatellaire du nerf saphène interne a été décrite, notamment par House. L’anatomie a montré qu’il pouvait exister des particularités anatomiques et notamment une importante angulation agressive au niveau du nerf autour du sartorius, voire une compression du nerf à travers une fente dans la portion musculotendineuse de ce muscle.
Diagnostic et traitement
La clinique, confortée par une échographie et un test anesthésique, pose le diagnostic.
La libération chirurgicale consiste à diviser partiellement le muscle sartorius et à déplacer le nerf à l’écart du site de piégeage. La compression se situe derrière le tendon du sartorius contre le condyle fémoral médial. Les résultats sont bons.
D’autres auteurs ont décrit des compressions du nerf saphène au niveau du canal de l’adducteur qui affectait la branche infrapatellaire de ce nerf.
Les pièges
Plusieurs auteurs ont décrit des pathologies prépatellaires dont le masque pouvait au moins, dans un premier temps, prêter à confusion.
Parmi ces diagnostics différentiels, il faut retenir les problèmes infectieux, notamment tuberculeux, les hémangiomes, les tumeurs à cellules géantes, les synovites villonodulaires et également toute la pathologie néoplasique, avec notamment les synovialo-sarcomes, les histiocytomes fibreux malins, les liposarcomes…
Conclusion
Il existe en avant de la rotule un certain nombre de structures anatomiques qui ont été décrites à la fois par les anatomistes et également par les imageurs. Entre les différentes couches, il existe trois espaces potentiels (bourses prépatellaires) en avant de la rotule. Les pathologies prépatellaires peuvent être diverses : le syndrome de Morel-Lavallée, l’hygroma ou la pseudo-bursite, la tumeur glomique, le syndrome de friction prépatellaire, la pathologie traumatique prépatellaire associée à des douleurs de type neurologique.
Bibliographie
• Arora S, Batra S, Rao S et al. A 40-year-old female with painless, slow growing prepatellar mass. J Clin Orthop Trauma 2014 ; 5 : 274-9.
• Bron A. Slow-growing Prepatellar Mass in a 31-year-old Woman Clin Orthop Relat Res. 2008 ; 466 : 1511-5.
• Claes T, Claes S, De Roeck J, Claes T. Prepatellar Friction Syndrome: A common cause of knee pain in the elite cyclist. Acta Orthop Belg 2015 ; 81 : 614-9.
• Clarsen B, Krosshaug T, Bahr R. Overuse injuries in professional road cyclists. Am J Sports Med 2010 ; 38 : 2494-501.
• Dye SF, Campagna-Pinto D, Dye CC et al. Soft-tissue anatomy anterior to the human patella. J Bone Joint Surg Am 2003 ; 85-A : 1012-7.
• House JH, Ahmed K. Entrapment neuropathy of the infrapatellar branch of the saphenous nerve. Am J Sports Med 1977 ; 5 : 217-24.
• Hosahalli G, Sierakowski A, Venkatramani H, Sabapathy SR. Entrapment Neuropathy of the Infrapatellar Branch of the Saphenous Nerve: Treated by Partial Division of Sartorius. Indian J Orthop 2017 ; 51 : 474-76.
• Huang YC, Yeh WL. Endoscopic treatment of prepatellar bursitis. Int Orthop 2011 ; 35 : 355-8.
• Ikpeme JO, Gray C. Traumatic prepatellar neuralgia. Injury 1995 ; 26 : 225-9.
• Kalthur SG, Sumalatha S, Nair N et al. Anatomic study of infrapatellar branch of saphenous nerve in male cadavers. Ir J Med Sci 2015 ; 184 : 201-6.
• Kerver AL, Leliveld MS, den Hartog D et al. The surgical anatomy of the infrapatellar branch of the saphenous nerve in relation to incisions for anteromedial knee surgery. J Bone Joint Surg Am 2013 ; 95 : 2119-25.
• Lapègue F, Sans N, Brun C et al. Imaging of traumatic injury and impingement of anterior knee fat. Diagn Interv Imaging 2016 ; 97 : 789-807.
• Nickerson TP, Zielinski MD, Jenkins DH, Schiller HJ. The Mayo Clinic experience with Morel-Lavallée lesions: establishment of a practice management guideline. J Trauma Acute Care Surg 2014 ; 76 : 493-7.
• Penaud A, Quignon R, Danin A et al. Alcohol sclerodhesis: an innovative treatment for chronic Morel-Lavallée lesions. J Plast Reconstr Aesthet Surg 2011 ; 64 : e262-4.
• Porr J, Chrobak K, Muir B. Entrapment of the saphenous nerve at the adductor canal affecting the infrapatellar branch – a report on two cases. J Can Chiropr Assoc 2013 ; 57 : 341-9.
• Schiefer TK, Parker WL, Anakwenze OA et al. Extradigital glomus tumors: a 20-year experience. Mayo clin Proc 2006 ; 81 : 1337-44.
• Silberman MR. Bicycling injuries. Curr Sports Med Rep 2013 ; 12 : 337-45.
• Tejwani SG1, Cohen SB, Bradley JP. Management of Morel-Lavallee lesion of the knee: twenty-seven cases in the national football league. Am J Sports Med 2007 ; 35 : 1162-7.

