LODA ou Lésions ostéochondrales du Talus : De leur physiologie à leur traitement
Les lésions ostéochondrales du dôme du talus deviennent un problème de plus en plus fréquent en traumatologie du sport. Il existe une réelle augmentation de la morbidité à court et long termes. Le diagnostic précoce est important. Les traumatismes directs ou indirects de la cheville en sont la cause la plus fréquente. Toutefois, des étiologies métaboliques, héréditaires sont souvent évoquées, surtout dans les lésions de la berge interne. Les améliorations de l’imagerie par scanner, arthroscanner, IRM, ainsi que l’arthroscopie, ont permis une meilleure approche diagnostique et thérapeutique de ces lésions. Le traitement médical est réservé aux lésions de petites tailles et supposées stables. Les autres bénéficient des techniques de microfractures. Ailleurs, les allogreffes, les greffes autologues de cartilage, voire les techniques de resurfaçage, sont proposées avec des résultats plus qu’intéressants.
Le talus est situé au centre de la cheville entre le tibia en haut, le calcaneus en bas et l’os naviculaire en avant. Son rôle est d’être répartiteur de forces entre la jambe et le pied. Il est donc soumis à des contraintes importantes lors de la marche et des activités sportives. Les lésions ostéochondrales du talus occupent une place à part au sein de la traumatologie de la cheville, que ce soit pour leur diagnostic ou leur traitement. Longtemps, leur terminologie fut confuse et l’étiopathogénie est restée un sujet controversé. Les indications thérapeutiques se précisent grâce à une meilleure analyse anatomo-clinique et aux progrès de l’imagerie.
ANATOMIE
Le talus est un os court formant le sommet de la voûte tarsienne. Il comporte trois segments : postérieur (le corps), antérieur (la tête), intermédiaire (le col). La face supérieure du corps est occupée (Fig. 1) par une surface articulaire en forme de poulie, convexe d’avant en arrière, concave transversalement. Plus large en avant qu’en arrière, elle s’articule avec le tibia. Si le talus est le siège d’insertions ligamentaires talofibulaire, tibiale et calcanéenne, il ne comporte pas d’insertion musculaire, ce qui explique la pauvreté de sa vascularisation. Il reçoit des rameaux terminaux de la tibiale postérieure, de la fibulaire et de la tibiale antérieure.
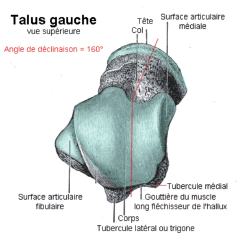
Figure 1 – Vue supérieure du talus gauche. Angle de déclinaison : 160 °.
LES CLASSIFICATIONS
Plusieurs classifications sont actuellement reconnues.
La FOG de Doré et Rosset (19)
La forme F (pour fracture) (Fig. 3)
Le fragment isolé n’est associé à aucune modification de la trame osseuse, condensation ou géode. Cette fracture peut être récente ou ancienne avec, dans ce cas, un aspect légèrement lytique. Dans la série des auteurs, cela représentait 18 % des cas, 87,5 % siégeaient sur le versant antérolatéral du talus, avec un antécédent traumatique constant.
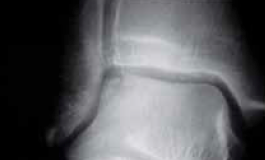
Figure 3 – La forme F.
La forme O (pour ostéonécrose)
(Fig. 4)
L’aspect est ici nécrotique avec séquestre, la trame osseuse sous-jacente est remaniée avec un liseré de condensation et microgéodes. Cela représente 75 % des cas, sans antécédent traumatique dans 66 % des cas et un siège postéro-médial au niveau du talus dans 70 % des cas.
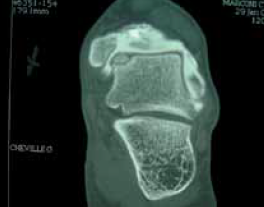
Figure 4 – La forme O.
La forme G (pour géode)
Elle est caractérisée par l’absence de fragment libre et de séquestre. En revanche, il existe une importante image radio-transparente intra-osseuse kystique (Fig. 5), à rapprocher des lésions kystiques de Kouvalchouk (13). Elles représentent 7 % de leurs cas, beaucoup moins que dans la série de Loomer (18). Toutefois, ces descriptions ne tiennent pas compte de l’état du cartilage qui conditionne les indications thérapeutiques et le pronostic.
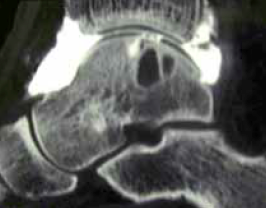
Figure 5 – Lésion géodique.
La classification de Ferkel
Ferkel (20) a alors proposé, au vu des images d’arthroscanner, qui donnent une analyse fine de l’état du cartilage, une classification en 5 stades :
- stade 1 : surface articulaire intacte, géodes sous-chondrales ;
- stade 2a : cartilage ouvert, géodes sous-chondrales ;
- stade 2b : cartilage ouvert, fragment non déplacé ;
- stade 3 : fragment non déplacé, géodes sous-chondrales ;
- stade 4 : fragment déplacé.
La classification de Mintz
Une évolution s’est faite en combinant les aspects IRM et arthroscopiques pour aboutir en 2003 à la classification proposée par Mintz (21). A partir d’une étude rétrospective de 54 cas, il propose une classification basée sur l’IRM en 5 stades qui ont une sensibilité de 95 %, une spécificité de 100 %, une valeur prédictive négative de 88 % et une valeur prédictive positive de 100 % avec des séquences IRM cartilagineuses particulières.
La classification comporte 6 stades :
- stade 0 : cartilage normal ;
- stade 1 : cartilage intact mais signal IRM anormal ;
- stade 2 : fissures ou lésions fibrillaires du cartilage mais os intact ;
- stade 3 : volet cartilagineux ou os sous-chondral exposé ;
- stade 4 : fragment cartilagineux libre non déplacé ;
- stade 5 : fragment libre déplacé.
Physiopathogénie
Les LODA représentent 0,06 % des fractures du talus et sont présentes dans environ 6 % des entorses de cheville. Le défaut et le retard de diagnostic sont fréquents pour atteindre près de 80 % dans les chevilles douloureuses chroniques post-entorse (22).
Les hypothèses concernant l’origine de ces lésions ostéochondrales sont nombreuses comme en attestent les multiples dénominations utilisées dans la littérature.
Il existe certes des formes traumatiques avec fracture cisaillement (11), mais également d’autres mécanismes non traumatiques, essentiellement pour les lésions médiales. Ces formes font penser à des étiologies vasculaires, synoviales ou métaboliques avec ou sans contexte microtraumatique. Des formes gémellaires (23) et familiales ont été rapportées.
Dans les formes F, un mécanisme par microcisaillement est admis. Mais dans les autres, le mécanisme est moins univoque. Dans les formes O, un fragment ostéo-cartilagineux se sépare du reste du talus. Le cartilage peut rester normal, continu ou se fissurer jusqu’à libérer ce fragment dans l’articulation. Un traumatisme, voire des microtraumatismes répétés, peuvent isoler ce fragment ostéochondral de son socle osseux. Il pourrait évoluer soit vers une libération d’un séquestre soit vers une consolidation (24). En faveur de cette évolution est la constatation de formes de passage entre les formes F et les formes O.
Lors d’un traumatisme en inversion, la contusion de l’angle postéro-médial peut entraîner, à la longue, une lésion de type O, le traumatisme initial pouvant être oublié.
L’hypothèse de l’hyperpression médiale qui ne met pas en jeu de traumatisme avec fracture pourrait expliquer le siège de ces lésions. Ces contraintes pourraient entraîner des microfractures de l’os souschondral avec apparition secondaire de lésion de type O ou d’une géode. Ceci expliquerait les lésions médiales sans antécédent traumatique et les lésions bilatérales survenant sur des morphotypes contraignants comme les arrière-pieds varus.
Les types G seraient secondaires à des contraintes importantes sur la face médiale du dôme talien. Ceci entraînerait des modifications vasculaires ou osseuses avec pour conséquence une nécrose de l’os sous-chondral comme dans les lésions de type O mais plus tard dans l’évolution. Ce type de lésion est évoqué lorsque l’on voit les anomalies IRM dans les traumatismes sans fracture.
On peut conclure que les formes F, le plus souvent latérales, sont d’origine traumatique alors que les formes O et G, plutôt médiales, résultent d’une autre cause et qu’il peut y avoir des formes de passage entre les formes F et O.
CLINIQUE
Devant tout tableau d’entorse grave de cheville, on doit envisager la survenue d’une fracture ostéochondrale du talus. Le gonflement, la survenue d’une ecchymose, une impotence marquée, la localisation des points douloureux, suffisent suivant les critères d’Ottawa pour imposer un examen radiologique qui mettra en évidence la zone de fracture. Il semble que près de la moitié des entorses ou fractures de cheville présentent des lésions de LODA. L’âge moyen se situe entre 20 et 30 ans avec une prépondérance masculine.
Dans les formes chroniques, l’examen s’attachera à préciser les circonstances de survenue, les suites immédiates, l’évolution de la symptomatologie. La clinique des LODA est sans surprise, il s’agit d’une cheville douloureuse avec limitation modérée des amplitudes articulaires. On recherchera les points douloureux en sachant que lors de la flexion plantaire forcée, on découvre la partie antérieure du talus. L’examen de la sous-talienne, du médiotarse et de la tarso-métatarsienne est indispensable.
On recherchera les mouvements anormaux en varus, un tiroir, un ballotement talien. On finira par les tests musculo-tendineux contre résistance. Le diagnostic va être complété par l’imagerie.
IMAGERIE
Les radiographies standard
(Fig. 6)
Indispensables, elles comprennent une incidence de face, en rotation médiale de 20° pour bien dégager le dôme talien et un profil. Il faut savoir, au moindre doute, demander un complément d’incidence par un trois quart déroulé de l’arrière-pied. En cas de négativité et si la clinique l’impose, il faut compléter l’imagerie standard.
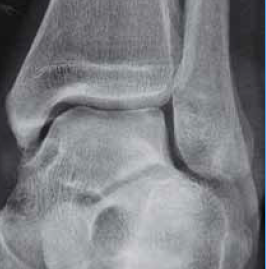
Figure 6 – Lésion de la berge extérieure.
La scintigraphie osseuse
(Fig. 7)
Beaucoup moins utilisée, elle peut exceptionnellement rester utile dans des douleurs inexpliquées de l’arrière et du médio-pied. Elle ne présente aucun intérêt dans l’analyse de la lésion.
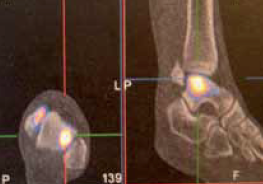
Figure 7 – Fixation sur talus.
Le scanner et l’arthroscanner
Plus que le scanner, l’arthroscanner (Fig. 8) était en France, jusqu’à récemment, l’examen de référence. Réalisé en coupes fines de 3 mm avec possibilité de reconstruction, il permet de préciser ou de confirmer une lésion soupçonnée sur les radios. Il précise la localisation d’un corps étranger, la profondeur et le siège exact d’un séquestre, d’une nécrose ou d’une géode. Quant au cartilage, une fissure, son siège, sa profondeur, ses rapports avec l’os sous-chondral sont précisés au mieux. Cet examen reste d’un apport important dans la décision thérapeutique.
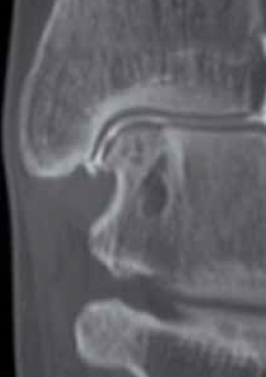
Figure 8 – Scanner.
L’IRM
(Fig. 9)
Elle ne permet pas, dans l’état actuel des choses, d’avoir une analyse aussi fine des lésions du cartilage que l’arthroscanner (25). Toutefois, son approche globale avec analyse de l’os (oedèmes osseux) et des parties molles (lésions ligamentaires) autorise dans les lésions médiales une meilleure approche de l’extension osseuse. Avantage que viennent compléter les données de l’arthroscanner. Gomol (26) considère que l’IRM sous-estime la taille des lésions cartilagineuses au niveau du genou, ce qui n’a pas été vérifié au niveau de la cheville mais qui doit être pris en compte dans le choix des indications thérapeutiques. D’après les travaux de Mintz (21), on peut considérer que l’IRM est en passe de devenir l’examen de référence permettant de mieux définir les indications opératoires. Yammine (27) souligne l’intérêt de l’IRM dans le diagnostic précoce des lésions du talus, associées ou non à des lésions ligamentaires, dans les suites des entorses graves de cheville. Elle permettrait de distinguer les formes “médicales” des formes “chirurgicales”. Elle peut être utile au suivi post-opératoire, la disparition du signal osseux évoquant une cicatrisation osseuse (28).
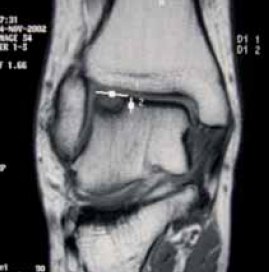
Figure 9 – Lésion forme G.
L’échographie
Proposée par Hattori (29) pour aider au diagnostic des lésions chondrales, elle reste d’un intérêt limité aux lésions antéro-externes. Les zones postérieures du talus sont le plus souvent des zones aveugles. Kaleva (30) trouve une corrélation faible pour quantifier les lésions et ne fait une distinction qu’entre le cartilage sain et le cartilage très altéré.
TRAITEMENT
Il importe qu’un diagnostic précoce soit posé afin de préserver l’avenir de la cheville. L’attitude thérapeutique doit être modulée en fonction du tableau clinique, du siège de la lésion, de son étendue en surface et en profondeur. Les indications restent délicates à poser, dépendant aussi de l’expérience de l’opérateur. Les excellents résultats, quelles que soient les techniques, avoisinent les 50 % sur un long recul. Il faut bien peser les indications en fonction de la motivation du patient, de la gravité des lésions, du retentissement et du risque thérapeutique.
Le traitement conservateur
Il peut être envisagé si la lésion est asymptomatique, pauci-symptomatique ou de très petite taille. Il consiste en une mise en décharge stricte avec botte de protection d’au moins 4 semaines en espérant une cicatrisation des lésions chondrales pures soit ostéo-cartilagineuses récentes, pas ou peu déplacées. Une surveillance radio-clinique permettra de suivre l’évolution locale et de savoir si un traitement chirurgical est indiqué en cas d’échec radio-clinique. Dans une revue de la littérature rapportée par Zengerink et al. (31) portant sur 52 études, seules 3 sont consacrées à la mise au repos avec décharge et antalgique, 4 avec en plus une immobilisation plâtrée. Le choix du traitement médical a été pris dans les anciennes études devant la méconnaissance du traitement chirurgical, par la suite l’alternative a été proposée aux patients en connaissance de cause. Environ 45 % de bons ou très bons résultats ont été rapportés avec un traitement conservateur sans que l’immobilisation plâtrée ait montré une supériorité.
Le traitement chirurgical
Les options sont nombreuses, elles ont pour but de restaurer un “cartilage” indolore par définition, il l’est par excision simple, par stimulation de l’os sous-chondral, enfin par greffes cartilagineuses ou ostéo-cartilagineuses. Techniquement que ce soit par chirurgie classique ou arthroscopique, on retient que les lésions latérales sont majoritairement abordables par une voie antérieure, une ostéotomie fibulaire est rarement nécessaire pour les lésions à extension postérieure. Les lésions médiales, le plus souvent postérieures, nécessitent le plus souvent une ostéotomie malléolaire médiale avec les aléas de consolidation que l’on connaît. Les techniques arthroscopiques développées depuis les années 1990, avec succès, permettent d’alléger les suites opératoires. Elles restent inadaptées aux formes supérieures à 1,5 cm2. Les voies d’abord postérieures permettent d’atteindre certaines lésions postéromédiales.
Indications
Dans les formes F (fractures)
Le traitement orthopédique peut être proposé dans les formes récentes, de petites tailles, pas ou peu déplacées. Ailleurs, le traitement chirurgical s’impose. Les fragments de grosses tailles peuvent être repositionnés et synthèsés ou collés (32) sous arthroscopie en fonction de l’expérience de l’opérateur. Les petits fragments sont simplement excisés et les fragments non déplacés sont immobilisés durant 4 semaines dans une botte d’immobilisation ou un plâtre. Les formes chroniques peuvent évoluer vers une libération du fragment avec un risque arthrogène ou vers une forme O par pseudarthrose et nécrose. L’arthroscanner et l’IRM précisent le siège et la taille du fragment. Les fragments libres seront excisés. Quand ils sont en place, l’attitude thérapeutique sera la même que pour les formes O.
Dans les formes O (ostéonécroses)
La décision sera prise en fonction de la taille, de la situation et de la profondeur de la lésion. Il n’y a pas de consensus dans la mesure où les excellents résultats, dans les différentes séries, dépassent difficilement les 50 %. Il faudra donc savoir s’abstenir, surtout si les lésions sont très profondes, étendues et postérieures et pauci-symptomatiques. Le geste opératoire comprendra (Fig. 10) l’excision des fragments libres, le curetage et l’excision des fragments nécrotiques et instables jusqu’en os saignant. Ensuite, en fonction de l’étendue, de la profondeur des lésions, on proposera différentes techniques.
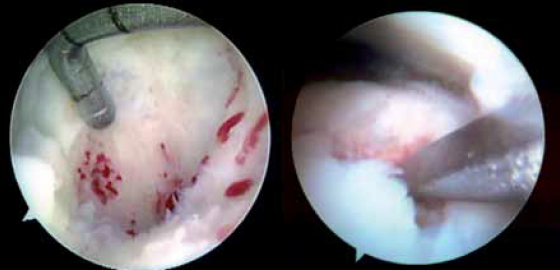
Figure 10 – Curetage.
• Les microfractures (Fig. 11), dans le cas de lésions de moins de 1,5 cm2 de surface, seront effectuées le plus souvent sous arthroscopie. Dans un premier temps, un débridement avec ablation des fragments cartilagineux libres ou mobiles, nettoyage des zones cartilagineuses au résecteur motorisé ou à la curette, jusqu’à l’os sous-chondral avec perforation à la pointe et non au moteur. Au lâcher du garrot, on constate un saignement par les pertuis osseux. Dans les suites, une marche en appui aidé de 2 à 4 semaines suivant la taille et le siège des lésions est conseillée. La reprise de la course est envisagée vers la 6e semaine et le sport vers 6 mois. Certains associent dans les suites une visco-supplémentation (33) ou l’injection de facteur de croissance sans que des études montrent une supériorité de ces traitements. Les différentes séries rapportent près de 90 % de bons et très bons résultats à 5 ans. Au-delà de 1,5 cm2, la pratique d’une greffe s’impose. Le type de greffe, autogreffe, allogreffe, thérapie cellulaire varie suivant les auteurs et dans le temps.
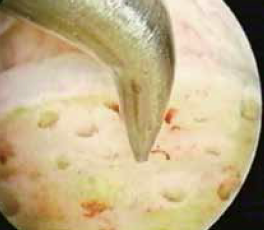
Figure 11 – Les microfactures sont le plus souvent effectuées sous arthroscopie.
• Les allogreffes fraîches ou congelées ont pour avantage d’éviter un site donneur chez le patient mais il existe des problèmes de tolérance immunologique et de survie du cartilage. Gross et al. (34) rapportent 9 cas d’allogreffes taliennes avec survie à 11 ans de 6 cas sur les 9.
• La greffe ostéochondrale autologue (Fig. 12) ou mosaicplasty (35) est réalisée par la mise en place d’un ou de plusieurs transplants autologues (36, 37). Initialement utilisée au niveau du genou, son utilisation a été étendue à la cheville sur des lésions unifocales de plus de 1,5 cm de diamètre. Le ou les greffons sont prélevés sur le genou homolatéral en zone non portante dans le même temps opératoire. Leur implantation se fera suivant leur taille et leur siège avec le plus souvent ostéotomie tibiale ou fibulaire. Une mise en décharge de 3 semaines, 6 pour ceux ayant eu une ostéotomie, est conseillée. Trois semaines d’appui aidé avec rééducation à visée mobilisatrice précèderont la mise en charge. Les activités sportives seront reprises vers 6 mois.
Les différentes publications (36) rapportent un taux de bons et très bons résultats de l’ordre de 90 % suivant les auteurs. Toutefois, la nécessité d’une ostéotomie au niveau de la cheville et de faire les prélèvements au niveau du genou homolatéral restent un frein pour certains en dépits de ces bons résultats. Une variante technique avec Kennedy et al. (38) qui utilisent une autogreffe ostéochondrale dont le greffon est au préalable “imbibé” de cellules souches issues de la moelle osseuse.
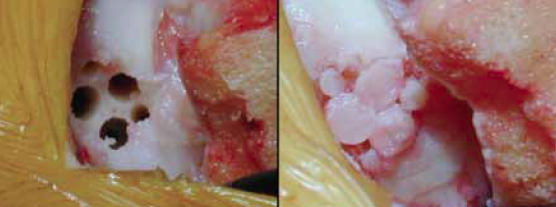
Figure 12 – Mosaicplasty avec ostéotomie malléolaire interne, avant et après mise en place des greffons.
• L’autogreffe, ou technique de régénération de cartilage, est dérivée de la technique de Brittberg (39) utilisée au genou depuis 1994. Contre-indiquée en cas de lésions dégénératives diffuses, dans les anomalies d’alignement de la cheville ou d’instabilité chronique, c’est une technique en deux temps. D’abord un prélèvement de 200 à 300 mg de cartilage est effectué au niveau de l’échancrure du genou homolatéral puis mise en culture. Quatre semaines plus tard, on met en place, au niveau de la lésion, la culture de chondrocytes recouverte par un clapet périosté. Dans certains cas, il est possible d’utiliser le fragment libéré comme source de cellules cartilagineuses, ce qui évite l’intervention pour prélèvement (40). Dans les suites, une mise en décharge est préconisée avec immobilisation stricte pendant deux semaines, puis avec port d’une botte d’immobilisation. La marche en appui aidé est autorisée avec le début d’une mobilisation passive progressive. La mise en charge se fait vers la 6e semaine. La course et les activités avec impulsion seront autorisées entre le 6e et 8e mois, la reprise du sport à un an. La couverture périostée et le comblement de la niche peuvent être remplacés par la mise en place d’une matrice 3D biodégradable. Cette matrice peut être composée de collagène type I/III porcine, de polydiaxanone/polyglactin ou d’acide hyaluronique. Cette matrice imprégnée de cultures de chondrocytes voire de PRP associés à des cellules médullaires préalablement séparées des hématies et du plasma va se réhabiter progressivement. Ne sont injectées que les cellules souches, monocytes lymphocytes et les autres cellules médullaires. Cette procédure prometteuse est en court d’évaluation.
• Le resurfaçage ou traitement par un implant métallique (HemiCAP, Arthrosurface Inc) du LODA (Fig. 13 et 14). Van Bergen et al. (41) rapportent le cas d’une femme de 20 ans sportive qui, dans les suites d’une entorse, développe une lésion du type kystique de la berge médiale. Elle a été traitée par 2 curetages arthroscopiques sans succès. Par abord médial avec ostéotomie malléolaire interne, la lésion est abordée et un implant métallique est mis en place. Elle reprend à un an son sport au même niveau et, avec deux ans de recul, elle continuait son sport sans problème. Cette technique est proposée pour des échecs des autres traitements, chez des sujets de plus de 18 ans sur les lésions inférieures à 20 mm. Les publications sont rares et quelques études cadavériques ont été rapportées (42).
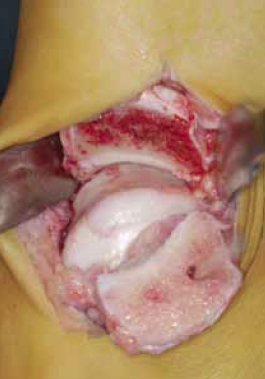
Figure 13 – Implant métallique recouvert par fibro cartilage (aut Dr Van Dijk).
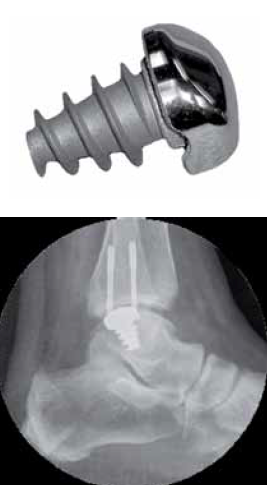
Figure 14 – implants et image radiologique.
Dans les formes G (géodes)
Asymptomatiques, elles seront respectées et surveillées.
Les lésions peu profondes sont traitées par curetage simple sous arthroscopie avec perforation jusqu’au saignement du fond de la cavité afin de favoriser le comblement par un fibrocartilage.
Les lésions profondes sont curetées et comblées avec du spongieux ou une matrice réhabitable comme cela a été mentionné pour les formes O avec de bons résultats cliniques et radiologiques. En cas de respect des surfaces cartilagineuses, l’abord de la zone de la lésion peut se faire, soit par voie transmalléolaire en perforant le cartilage du dôme du talus, soit par voie rétrograde.
D’après les travaux de Taranow (43), il est préférable d’aborder la lésion par voie rétrograde. Le positionnement est précisé par l’imagerie standard et l’IRM puis contrôlé en peropératoire sous amplificateur de brillance en montant une broche qui servira de guide vers la niche pathologique en respectant les surfaces cartilagineuses. Dans les suites, une mobilisation précoce est conseillée en restant en décharge pendant 4 semaines. Une mise en charge partielle est ensuite autorisée avant la mise en charge complète vers la 62 semaine. Le footing est permis vers 3 mois et les activités sportives vers le 62 mois. Kono (44) rapporte une dégradation des images IRM à un an chez les patients ayant eu un traitement transmalléolaire dans 42 % des cas alors que, dans la voie rétrograde qui épargne le cartilage, aucune altération n’est apparue à un an.
CONCLUSIONS
Le choix du traitement dépend de nombreux facteurs : l’âge, les douleurs, leur durée d’évolution, la localisation et la profondeur de la lésion.
Les lésions asymptomatiques ou peu gênantes sont traitées par le repos, la mise en décharge, une botte d’immobilisation pendant une durée de 4 à 6 mois. Près de 50 % des cas guérissent et ce délai ne ferme pas la porte aux traitements chirurgicaux. Il est toujours temps de se tourner vers la chirurgie (45). Celle-ci est envisagée en cas d’échec du traitement médical ou devant la persistance de symptômes après une première intervention. Les différents travaux nous incitent à proposer d’abord un geste combinant un “débridement” lésionnel avec microfractures si les lésions sont trop petites pour envisager une remise en place du fragment.Par conséquent, les lésions de moins de 1,5 cm2 reçoivent ce traitement même s’il s’agit d’une forme kystique.
Dans les formes kystiques au-delà de 1,5 cm2, après “débridement”, une greffe osseuse peut être mise en place pour boucher la niche. Si le cartilage surplombant la niche est intacte, la niche est traitée par voie rétrograde avec bourrage de spongieux prélevé le plus souvent sur la crête iliaque ou sur le tibia. La fixation du fragment est réalisée si la taille de celui-ci est supérieure à 15 mm ou chez les adolescents en cas de faillite du traitement médical.
En cas d’échec de ces traitements, on se portera vers les greffes autologues de cartilage par mosaicplasty ou par greffes autologues de cartilage. Ces techniques ont pour but de restaurer un vrai cartilage sur la zone pathologique.
La mosaicplasty, bien que séduisante, se heurte aux problèmes du site donneur le genou, l’absolue nécessité de faire une ostéotomie tibiale ou fibulaire pour bien aborder le site receveur. Il semble que dans l’avenir le remplacement de ces autogreffes par des matériaux réhabitables, voire des implants métalliques, puisse alléger la procédure.
Les greffes autologues de culture de cartilage sont pleines de promesses mais le recul n’est pas encore suffisant pour connaître les résultats à long terme de cette technique à la cheville. Dans les formes étendues, certains ont proposé des allogreffes mais les reculs ne sont pas suffisants pour proposer ce type d’intervention en première intention. Malheureusement, en cas d’échecs itératifs ou d’atteintes massives, une chirurgie prothétique ou une arthrodèse peuvent être proposées.
HISTORIQUE
1558 : A. Paré fut le premier à rapporter l’ablation d’un corps étranger d’une articulation (1).
1738 : Monro décrit une lésion ostéochondrale avec libération de corps étrangers dans les suites d’un traumatisme de cheville (2).
1854 : Broca évoque une ostéonécrose avec libération secondaire d’un fragment au niveau du genou (3).
1879 : Paget rapporte deux cas de libération de corps étrangers dans des genoux (4) et c’est en 1887 que König parle d’ostéochondrite disséquante comme étant une ostéonécrose spontanée, faisant référence aux lésions du genou (5).
1922 : Kappis décrit un cas de corps étranger de cheville et parle lui aussi d’ostéochondrite disséquante (6).
1932 : Rendu décrit une « fracture parcellaire intraarticulaire de la poulie astragalienne » (7).
1933 : Fairbank affirme qu’un traumatisme est à l’origine de troubles vasculaires de l’os sous-chondral entraînant une nécrose avasculaire, « l’osteochondritis dissecans » (8). Depuis cette époque, la physiopathologie de ces lésions ostéochondrales de l’astragale reste sujet à controverse. On va parler alternativement d’ostéochondrite disséquante, de fractures ostéochondrales, d’ostéochondrite juvénile, d’ostéochondrite primitive, de nécrose partielle de l’astragale, de fractures ostéochondrales, partielles, du dôme… Les Anglo-Saxons ne seront pas en reste, évoquant des « flake fracture ou chip fracture, osteochondritis dissecans », ces différentes terminologies étant toujours valides dans les recherches bibliographiques. Ce flou entourant la physiopathologie n’a pas été levé par Soeur qui en 1950 rapporte la première « ostéochondrite disséquante » française de la cheville, d’origine post-traumatique (9).
1953 : Röden rapporte 55 cas personnels (10). Il est le premier à considérer les lésions externes comme post-traumatiques et les lésions internes comme spontanées, d’origine métabolique ou faisant suite à des microtraumatismes.
1959 : Berndt et Harty rassemblent les 191 cas publiés dans la littérature en plus de leur série de 24 cas (11). Ils pensent que les lésions internes et externes sont des fractures ostéochondrales et que ce sont des fractures parcellaires plus ou moins évoluées. Ils les classent en 4 stades radio-cliniques (Fig. 2) :
– stade I, compression avec modification localisée de la trame osseuse sans fragment individualisable ; – stade II, fragment ostéochondral partiel ;
– stade III, fragment détaché mais en place dans sa niche ;
– stade IV, fragment libre, niche vide.
1977 : Metges distingue les fractures ostéochondrales et les ostéochondroses disséquantes de l’astragale en séparant sur le plan radiographique les ostéochondroses dont l’angle de raccordement niche surface articulaire est aigu et forme un bec des fractures ostéochondrales pour lesquelles l’angle de raccordement du foyer de fracture est obtus et ne forme pas de bec (12). En fait, cette distinction se heurte à de nombreux problèmes.
1984 : C’est à Kouvalchouk que l’on doit l’introduction du terme de LODA, en remplacement du terme impropre d’ostéochondrite disséquante (13). Il décrit les formes kystiques.
1986 : Parisien (14) puis Pritsch (15) ont été les premiers à décrire le traitement arthroscopique de ces lésions, suivis par Frank dès 1988 (16).
1990 : Gérard rassemble 102 cas et confirme que nombre de ces lésions sont atraumatiques puisque dans 6 cas il retrouve des lésions bilatérales et dans 6 autres des “ostéochondrites” dans d’autres articulations (17). Chez ces 12 patients, ces lésions siégeaient sur la berge interne de la trochlée.
1993 : Loomer, ne pouvant classer ses 92 cas dans les 4 stades de Berndt et Harty, en crée un cinquième : les formes kystiques qui représentent 73 % de ses cas (18).
1995 : Il faut reconnaître à Doré et Rosset d’avoir proposé, en étudiant une série de 169 cas de la Société Orthopédique de l’Ouest (SOO), une nouvelle classification dite “FOG”, reposant sur l’aspect des lésions (fracture, ostéonécrose, géode) et sur les rapports de la lésion avec le corps du talus (situation par rapport à la surface, condensation autour du fragment) (19).

Figure 2 – Classification Berndt et Harty.
Pour en savoir plus
- Paré A. OEuvres complètes. Paris : J.B. Ballière, 1840-1841 ; 3 : 32.
- Munro A. Part of the cartilage of the joint separated and ossified. Medical Essays and Observations 1738 ; 4 : 19.
- Broca P. Sur la nécrose des cartilages articulaires. Aerzte in Paris. 1854 ; 38.
- Paget J. On the production of some loose bodies in joints. St Bartholomew’s Hosp Reports 1870 ; 6 :1-4.
- König F. Ueber frei körper in den Gelenken. Deutsche Zeitscher F Chir 1888 ; 27 : 90-109.
- Kappis M. Weltere beltragezur traumatisch-mechanischen entstehung der spontanen knorpelablosungen. DeutschZ Chir 1922 ; 171 : 13-29.
- Rendu A. Fracture intra-articulaire parcellaire de la poulie astragalienne. Lyon Med 1932 ; 150 : 220.
- Fairbank HAT. Osteochondritis dissecans. British J Surg 1933 ; 21 : 67-82.
- Soeur R. Osteochondrite disséquante de la cheville. Acta orthop Belgica1950 ; 16 : 493-502.
- Röden S, Tillegard P, Unnander-Scharin L. Osteochondritis dissecans and similar lesions of the talus. Acta Orthop Scand 1953 ; 23 : 51.
- Berndt AL, Harty M. Transchondral fractures (osteochondritis dissecans) of the talus. J Bone Joint Surg 1959 ; 41 : 988.
- Metges PJ, Delahaye RP, Minne J et al. Un signe radiologique intéressant dans le diagnostic différentiel : ostéo- chondrite disséquante— fracture parcellaire de l’astragale. Med Arm 1977 ; 5 : 555-8.
- Kouvalchouk JF, Watin-Augouard L, Schneider-Maunoury G. Lésions ostéochondrales du dôme astragalien. Traitement par curetage et comblement. J Trauma Sport 1993 ; 10 : 212-6.
- 14. Parisien JS. Arthroscopic treatment of osteochondral lesions of the talus. Am J Sports Med 1986 ; 211-7.
- Pritsch M, Horoshovski H, Farine I. Arthroscopic treatment of osteochondral lesions of the talus. J Bone Joint Surg (Am) 1986 ; 68 : 862-5.
- Frank A, Cohen P, Beaufils P, Lamare JP. Traitement arthroscopique des lésions ostéochondrales du dôme astragalien. Rev Chir Orthop 1988 ; 74 (Suppl. II) : 233-7.
- Gérard Y, Bernier JM, Ameil M. Lésions ostéochondrales de la poulie astragalienne. Rev Chir Orthop 1989 ; 75 : 466-78.
- Loomer R, Fischer C. Osteochondral lesions of the talus. Am J Sports Med 1993 ; 21 : 13-9.
- Dore JL, Rosset P. Lésions ostéochondrales du dôme astragalien. Étude multicentrique de 169 cas. Ann Orthop Ouest 1995 ; 27 : 146-91.
- Ferkel RD, Sgaglione NA, Del Pizzo W et al. Arthroscopic treatment of osteochondral lesions of the talus: technique and results. Orthop Trans 1990 ; 14 : 172.
- Mintz DN, Tashjian GS, Connell DA et al. Osteochondral lesions of the talus: a new magnetic resonance grading system with arthroscopic correlation. Arthroscopy 2003 ; 19 : 353-9.
- White KS. Sands AK. Osteochondral lesions of the talus associated with ankle fractues. Foot Ankle 2009 ; 20 : 123-9.
- Woods K, Harris I. Osteochondritis dissecans of the talus in identical twins. J Bone Joint Surg Br 1995 ; 77 : 331.
- Cox HA, Kuwade GT. Transchondral fractures of the talar dome. Clin Podiatr Med Surg 1995 : 667-87.
- Verhagen RA, Mass M, Dijkgraaf MGW et al. Prospective study on diagnostic strategies in osteochondral lesions of the talus. Is MRI superior to helical CT? J Bone Joint Surg Br 2005 ; 87 : 41-6.
- Gomol H, Yoshioka, Watanabe A et al. Preoperative measurement of cartilage défects by MRI underestimates lésion size. Cartilage 2011 ; 2 : 389-93.
- Yammine K, Fathi Y. Ankle “sprains” during sport activities with normal radiographs: incidence of associated bone and tendon injuries on MRI findings and its clinical impact. Foot 2011 ; 21 : 176-8.
- Higashiyama I, Kumai T, Takakura Y, Tamail S. Follow-up study of MRI for osteochondral lesion of the talus. Foot Ankle int 2000 ; 21 : 127-33.
- Hattori K, Kumai T, Takakura Y, Ikeuchi K. Ultrasound evaluation of cartilage damage in osteochondral lesions of the talar dome and correlation with clinical etiology: a preliminary report. Foot Ankle Int 2007 ; 28 : 208-13.
- Kaleva E, Saarakala S, Toyras J et al. In vitro comparaison of Timedomain, fréquency-domain and wavelet ultrasons parameters in diagnostics of cartilage dégénération. Ultrasons Med Biol 2008 ; 34 : 155-9.
- Zengerink M, Struijs P, Tol J, Van Dijk CN. Treatment of osteochondral lesions of the talus: a systematic review. Knee Surg Sports Traumatol Arthrosc 2010 ; 18 : 238-46.
- Kelbérine F, Frank A. Arthroscopic treatment of osteochondral lesions of the talar dome: a retrospective study of 48 cases. Arthroscopy 1999 ; 15 : 77-84.
- Doral MN, Bilge O, Batmaz G et al. Treatment of osteochondral lesions of the talus with microfracture technique and post opérative injection. Knee Surg Sports Traumatol Arthrosc 2012 ; 20 : 1398-403.
- Gross AE, Agnidis Z, Hutchinson CR. Osteochondral defect of the talus treated by fresh osteochondral allograft transplantation. Foot Ankle Int 2001 ; 22 : 385-91.
- Hangody L, Kish G, Karpati Z et al. Treatment of Osteochondritis Dissecans of the Talus: Use of the Mosaicplasty Technique—A Preliminary Report. Foot Ankle 1997 ; 18 : 628.
- Versier G, Christel P, Bures C et al. Traitement des lésions cartilagineuses du dôme de l’astragale par autogreffes ostéochondrales en mosaïque. e-mémoires de l’Académie nationale de chirurgie 2005 ; 4 : 1-11.
- Christel P. Versier G, Landreau Ph, Djian P. Les greffes osteo-chondrales selon la technique de la mosaicplasty. Maitrise Orthopédique 1998 ; 76 ; 1-13.
- Kennedy J, Murawski C. The treatment of osteochondral lesions of the talus with autologous osteochondral transplantation and marrow aspirate concentrate: surgical technique. Cartilage 2011 ; 2 : 327-36.
- Brittberg M, Lindahl A, Nilsson A et al. Treatment of Deep Cartilage Defects in the Knee with Autologous Chondrocyte Transplantation. N Engl J Med 1994 ; 331 : 889.
- Vannini et All ICRS congrès 2010 – Sitges. poster
- Van Bergen CJ, Reilingh ML, Van Dijk CN. Tertiary osteochondral defect of the talus treated by a novel contoured metal implant. Knee Surg Sports Traumatol Arthrosc 2011 ; 19 : 999-1003.
- Van Bergen CJ, Zengerink M, Blankevoort L et al. Novel metallic implantation technique for osteochondral defects of the medial talar dome. A cadaver study. Acta Orthop 2010 ; 81 : 495-502.
- Taranow WS, Bisignani GA, Towers JD, Conti SF. Retrogradedrilling of osteochondral lesions of the medial talar dome. Foot Ankle Int 1999 ; 20 : 474-80.
- Kono M, Takao M, Naito K et al. Retrograde Drilling for Osteochondral Lesions of the Talar Dome. Am J Sports Med 2006 ; 34 : 1450.
- Laffenetre O. Lésions Ostéochondrales du Talus. RCO Traumat 2010 ; 96 : 629-43.

